Электроотрицательный атом
Cтраница 3
Образование положительных ионов из электроотрицательных атомов было бы, очевидно, связано с чрезмерной затратой работы и поэтому может происходить лишь в исключительных случаях; то же самое действительно и для образования отриц. [31]
Центр системы координат соответствует менее электроотрицательному атому. В случае необходимости на рисунках и в таблице изменены обозначения оригинальных работ во избежание путаницы. [32]
В соединениях кремния с электроотрицательными атомами, имеющими неподеленную пару, происходит делокализация электронов с электроотрицательного атома на вакантные Зй-орбиты кремния. [33]
Если два заместителя с электроотрицательным атомом, присоединенным к кольцу, расположены в мета-положении по отношению друг к другу, то находящийся между ними атом водорода особенно легко замещается на металл. [34]
Образование водородных связей между электроотрицательными атомами или я-электронами молекул адсорбируемого вещества и атомами водорода силанольных групп на поверхности кремнезема играет основную роль в процессе адсорбции молекул из пара или неводного раствора. Образование водородных связей оказывается также главным фактором при адсорбции недиссоциированных молекул из водного раствора. [35]
Водородные связи возникают между электроотрицательными атомами молекул ( например, О, N) за счет атомов водорода, как бы связывающих молекулы. [36]
При образовании связей с менее электроотрицательными атомами ( для фтора это - все элементы, для хлора - все, кроме фтора и кислорода) валентность всех галогенов равна. Положительные степени окисления невоз-можны для фтора. Примеры соединений приведены в Справочной части. [37]
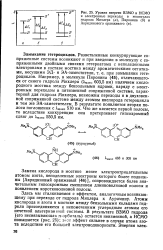 |
Уровни энергии ВЗМО и НСМО и электронные переходы в молекулах гидрола Михлера ( а, Пиронина ( б и Акридинового оранжевого ( в. [38] |
Замена кислорода в мостике менее электроотрицательным атомом азота, неподеленные электроны которого более подвижны [ Акридиновый оранжевый ( 46) ], сопровождается более значительным гипсохромным смещением длинноволновой полосы и появлением коротковолновой полосы. [39]
Водородные связи характерны лишь для электроотрицательных атомов, таких, как фтор, кислород, азот. Этими связями объясняются необычные свойства воды. [40]
Положительный протон притягивается электродными оболочками электроотрицательных атомов, даже внедряется в них. Вследствие этого и возникает довольно прочная дополнительная связь, получившая название водородной. [41]
Положительный протон притягивается электродными оболочками электроотрицательных атомов, даже внедряется в них. Вследствие этого и возникает довольно прочная дополнительная связь, получившая название водородной. [42]
Отдельно следует рассмотреть случай адсорбции электроотрицательных атомов, например кислорода, на поверхности полупроводника. В большинстве случаев такие адсорбированные атомы имеют свободные уровни, расположенные значительно ниже зоны проводимости, поэтому у поверхности возникают явления, уже рассмотренные в § 4 в связи с поверхностными состояниями. Благодаря наличию положительного объемного заряда энергетические уровни собственного полупроводника у поверхности могут сильно сместиться, В результате заполненная зона может настолько подняться, что электроны из нее начнут переходить на атомы кисло-рода, создавая дырки в заполненной зоне. [43]
Метильные группы, присоединенные к электроотрицательному атому. Изучение таких соединений, как СС13 - СООСН3 [6, 9] и CD3COOCH3 [10], у которых водородные атомы присутствуют только в метальных группах, показывает, что мето-ксигруппа дает в области валентных колебаний СН также картину из пяти полос. Мнения об отнесении отдельных полос различны, однако типичные интервалы в соответствии с отнесением Жозьен и др. [1, 6, 9] приведены ниже. Существуют четкие отличия от соответствующих частот ароматических соединений, особенно для более низкочастотных полос. [44]
 |
Энергия межатомных связен.| Кривые потенциальной энергии межатомных и межмолекуляр-ных взаимодействий. а - ковалент-ная связь. б - водородная связь. в - ван-дер-ваальсово взаимодействие. [45] |
Страницы: 1 2 3 4