Кристалл - сульфит
Cтраница 1
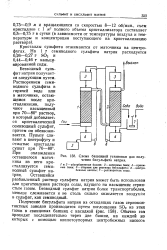 |
Схема башенной установки для получения бисульфита натрия. [1] |
Кристаллы сульфита отжимаются от маточника на центро-фугах. На 1 т семиводного сульфита натрия расходуется 0 26 - 0 27 т SO2 и 0 44 - 0 46 т кальцинированной соды. [2]
 |
Схема магнезитового бескристального метода очистки газов от SO2. [3] |
Кристаллы сульфита цинка выпадают в осадок, их отделяют от жидкости фильтрацией или центрифугированием. Отфильтрованный ZnSO3 2 5Н2О при нагревании до 300 - 350 С разлагается на Н2О, SO2 и ZnO. Окись цинка возвращается в цикл поглощения, a SO2 выдается в виде продукта. Сульфит цинка, образующийся побочно, окисляется кислородом воздуха в сульфат, который остается в растворе. Сульфат цинка может быть переработан различными способами. [4]
Кристаллы сульфита цинка отделяют фильтрацией или центрифугированием и разлагают при 300 - 350 С на Н2О, SO2 и ZnO. Оксид цинка возвращают в процесс. [5]
Кристаллы сульфита магния разлагаются путем обжига на SO2 ( получается в виде газа концентрации около 13 %) и MgO, которая возвращается в процесс. [6]
На кристаллы сульфита натрия подействовали серной кислотой и обнаружили, что идет выделение бесцветного газа с резким запахом. [7]
На кристаллы сульфита натрия подействовали серной кислотой и обнаружили, что идет выделение бесцветного газа с резким запахом Когда в поток газа ввели влажную лакмусовую бумажку, она покрасне ла При смешивании газа с влажным сероводородом появился желтоватый туман О каком газе здесь идет речь. [8]
К нескольким кристаллам сульфита натрия приливают 1 - 2 мл разбавленной серной кислоты и осторожно нюхают раствор. О каком свойстве сернистой кислоты свидетельствуют наблюдения. [9]
На дно колбы насыпьте кристаллы сульфита натрия так, чтобы нижний конец воронки был полностью погружен в порошок. [10]
Поместите 3 - 4 кристалла сульфита натрия в сухую пробирку и, закрепив ее в штативе, нагревайте в пламени горелки в течение 4 - 5 мин. [11]
Поместите 3 - 4 кристалла сульфита натрия в сухую пробирку и, закрепив ее в штативе, нагрейте в пламени горелки в течение 4 - 5 мин. [12]
Сухую пробирку с несколькими кристаллами сульфита натрия закрепляют в штативе и осторожно нагревают 5 - 6 мин. Пробирке дают остыть, вливают 1 мл дистиллированной воды и перемешивают. Добавляют понемногу раствор сульфата меди. Чем объясняется образование осадка черного цвета. Что является окислителем, что восстановителем в первой реакции. [13]
По имеющимся данным, рост кристаллов сульфита натрия существенно зависит от содержания в растворах ионов железа. Однако реальная возможность уменьшить содержание железа в растворах до такой степени, чтобы проводить кристаллизацию собственно сульфита натрия, представляется лишь в случае разделения во времени процессов получения насыщенного по сульфиту натрия раствора и кристаллизации из него целевой соли. Раствор сульфита натрия может быть очищен от примесей железа и других тяжелых металлов подщелачиванием раствором каустической соды с переводом примесей в нерастворимый гидроксид. Раствор далее очищают от выделившегося осадка простым отстаиванием. [14]
 |
Диаграмма состояния системы SO3 - Н2О. [15] |
Страницы: 1 2 3 4