Галоидный атом
Cтраница 2
У всех галоидных атомов при образовании ординарных ко-валентных связей остаются по две пары неподеленных валентных электронов. [16]
Реакционная способность галоидных атомов, находящихся в а-положении по отношению к карбонильной группе, зависит от природы галоида. Хлорпроизводные кетонов кислот, сложных эфиров и нитрилов не реагируют при комнатной температуре, между тем как соответствующие се-бром - и а-иодпроизводные реагируют немедленно. Простые j - хлор и - бромэфиры обладают аномальной реакционной способностью [47] и не образуют осадка при действии спиртового раствора азотнокислого серебра. Галоиды в а-галоидзамещенных кетонах легко удаляются при действии щелочных реактивов, например спиртового раствора едкого кали или водного раствора уксуснокислого натрия. Если элементарный анализ указывает на присутствие галоида, а со спиртовым раствором азотнокислого серебра соединение дает отрицательную реакцию, то рекомендуется прокипятить в течение 10 мин. Затем смесь разбавляют двойным объемом десгиллированной воды, охлаждают, подкисляют разбавленной азотной кислотой и фильтруют. Бели фильтрат мутный, его осветляют, приливая 1 - 2 капли этилового спирта, и прибавляют раствор азотнокислого серебра. При этом изменении способа должна получаться положительная реакция с такими соединениями, как ш-хлораце-тофенон, который не дает осадка непосредственно со спиртовым раствором азотнокислого серебра. [17]
Реакционная способность галоидного атома в органических соединениях зависит от взятого реактива. [18]
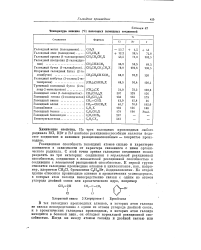 |
Температура кипения ( С некоторых галоидных соединений. [19] |
Реакционная способность галоидных атомов сильно и характерно изменяется в зависимости от характера связанного с ними органического радикала. [20]
Соединения с галоидным атомом в а-положении к сульфоновой группе имеют интересные свойства. В то время как реакции двойного обмена для этих соединений проходят с трудом, замещение галоида водородом происходи значительно легче, чем для галоидалкилов. [21]
Кроме того, галоидные атомы, стоящие у соседних угле родов, по крайней мере в некоторых случаях, могут быть отняты при помощи хинолина тг. [22]
Атомы отдачи замещают галоидные атомы, атомы водорода и атомные группы в молекулах галоидорганических соединений. Основная часть атомов отдачи распределяется между исходным химическим соединением и свободным галоидом. Так как периоды полураспада указанных выше изотопов малы, а сечения реакций велики, то при кратковременном облучении получается материнское вещество с высокой удельной активностью. Этим путем могут быть получены любые галоидорганические соединения. В производственной практике так получают бромбензол, однако прямое облучение требует последующей очистки. [23]
Гидроксильная группа и галоидный атом галоидгидринов обладают нормальной реакционной способностью. [24]
При увеличении числа галоидных атомов в молекуле ее удельный вес увеличивается. Соединения, содержащие два или более атомов хлора или один атом хлора вместе с атомом кислорода или арильной группой, вообще имеют удельный вес больше единицы. [25]
Для преимущественного вхождения галоидного атома в фенолы в орто - или пара-место имеет невидимому наибольшее значение температура. Поиышение ее содействует орто-орнентации. [26]
В галоидпроизводных последнего типа галоидный атом ведет себя так же, как и в галоидпроизводных жирного ряда. [27]
Значительно большей подвижностью обладает галоидный атом в дн-нитросоединениях. [28]
Гораздо большей подвижностью обладает галоидный атом в ди-нитросоединениях, и соответственно реакция идет значительно энергичней. [29]
В галоидпроизводных последнего типа галоидный атом ведет себя так же, как и в галоидпроизводных. [30]
Страницы: 1 2 3 4