Кристаллизант
Cтраница 2
Диполь-ный момент цпол обусловлен деформацией ионов кристаллизанта. Такая деформация вызвана как непосредственным действием электрического поля, изменяющего распределение электронной плотности вокруг ядер ионов, так и вторичным эффектом - смещением ионов под влиянием поля. [16]
При внешнедиффузионном режиме кристалл сорбирует примесь и кристаллизант из среды так быстро, что ее состав не успевает выравниться. Поэтому для определения концентраций Сг и С необходимо знать, как распределена примесь по всей системе. Эксперименты показали [97-98], что такое распределение резко зависит от геометрии кристалла, от формы кристаллизатора и мешалки, от характера движения среды. [17]
Коэффициенты равновесного распределения примеси между твердой фазой кристаллизанта и его растворами в разных растворителях описываются формулой Ратнера при значении AfiTJ -, не зависящем от свойств жидкой фазы. [18]
Ск 1; pi - число молекул кристаллизанта, дополнительно вовлекаемых в ближайшую координационную сферу молекулы i-формы при превращении ее в i -форму. [19]
 |
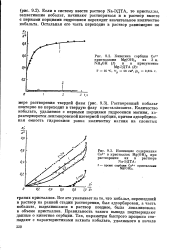
Результаты исследования распределения 1Вг между кристаллами и паром иода. [20] |
Рк и Рп - давление насыщенного пара кристаллизанта и примеси при температуре сокристаллизации Т; f5 - разрывная функция, принимающая значения р 0 при Т Т - пл и Р 1 при Т Тпл; ДЯПл и Тпл - энтальпия и температура плавления ( 38 2 С) йодистого брома; AZ - эмпирический параметр, приведенный в табл. 13; Д2 17 2 кДж / моль и Pz 5 4 ( 0 5) 10 - 2 - кДж / ( моль А) - эмпирические коэффициенты. [21]
 |
Кинетика сорбции Со2.| Изменение содержания. [22] |
Растворенный кобальт повторно не переходит в твердую фазу кристаллизанта. [23]
При образовании соединения включения происходит изменение первоначальной структуры кристаллизанта, например, карбамид изменяет тетрагональную структуру на гексагональную, но после удаления включенного компонента водородные связи снова сдвигают молекулы карбамида в менее открытую структуру - тетрагональную. [24]
 |
Электронная микрофотография скола гранулы аммофоса на основе фосфорной кислоты из фосфоритов Каратау ( увеличение Х20000. [25] |
Другой особенностью этого процесса является существенная неоднородность концентрации кристаллизанта в растворе. [26]
 |
Схема направленной кристаллизации. [27] |
Однако в общем случае для поддержания постоянной концентрации кристаллизанта необходимо увеличивать скорость Av, тем самым компенсируя ускорение кристаллизации из-за увеличения поверхности твердой фазы. [28]
Правило Руффа утверждает, что если отношение растворимостей кристаллизанта и примеси больше единицы, то твердая фаза обогащается примесью, если же меньше - то обедняется. Это правило, согласно данным, приведенным на рис. 8.8, выполняется при равновесии с точностью до полупорядка. [29]
Различие температуры крупных и мелких кристаллов усиливается, если кристаллизант участвует в химических реакциях, протекающих в фазах системы или на ее стенках. Неоднородность распределения температур, напряжений и дефектов в объеме фаз приводит к неоднородности распределения энтропии, внутренней энергии и энергии Гиббса [ 1, с. Поэтому при анализе соосаждения необходимо учитывать неоднородность распределения любого экстенсивного свойства фаз системы и возможность появления источников этого свойства в объеме фаз, на поверхности кристаллов и на стенках системы. При таком анализе раствор ( пар) следует рассматривать как дисперсионную среду, а кристаллы - как дисперсную фазу, частицы которой связаны непрерывной функцией распределения по состояниям. Внутренние и внешние обобщенные координаты связаны с обобщенными силами ( химическим потенциалом, напряженностью электрического и магнитного поля, мощностью радиационного поля, силой тяготения, механическим напряжением и температурой) уравнениями состояния дочерней и материнской фаз. Изменение внутренних обобщенных координат определяется законами переноса массы и энергии в объеме кристаллов и условиями массо - и энергообмена материнской и дочерней фаз. [30]
Страницы: 1 2 3 4