Кристаллизация - нитрат - кальций
Cтраница 2
В нейтрализаторы 17 вместе с маточным раствором подают некоторое количество азотной кислоты для выравнивания отношения N: пДь так как часть азота была удалена из вытяжки при кристаллизации нитрата кальция. При его нейтрализации до рН 3 5 - г - - т - 3 8 выделяется осадок, состоящий иЗ дикальцийфосфата с примесью небольших количеств трикальцийфосфата. [16]
 |
Схема производства азофоски. [17] |
В нейтрализаторы 17 вместе с маточным раствором подают некоторое количество азотной кислоты для выравнивания отношения N: Р2О5, так как часть азота была удалена из вытяжки при кристаллизации нитрата кальция. При его нейтрализации до рН 3 5 - 3 8 выделяется осадок, состоящий из дикальций-фосфата с примесью небольших количеств трикальцийфосфата. [18]
Из азотнокислотной вытяжки, полученной разложением фосфата 5 % - ным избытком 50 - 53 % - ной азотной кислоты ( в расчете на СаО), после кристаллизации нитрата кальция при - 15 фильтрат содержит [24]: 18 - 21 % Р20В, 5 5 - 6 5 % СаО, 4 5 - 5 5 % азота ( общ. [19]
В нейтрализаторы 17 вместе с маточным раствором подают некоторое количество азотной кислоты для выравнивания отношения N: Р205, так как часть азота была удалена из вытяжки при кристаллизации нитрата кальция. Протекающий непрерывно через ряд нейтрализаторов раствор содержит в качестве основных компонентов Н3Р04, Ca ( N03) 2 и HN03 - При его нейтрализации до рН 3 5 - f - 3 8 выделяется осадок, состоящий из дикальцийфосфата с примесью небольших количеств трикальцийфосфата. Кроме того, в осадке содержатся небольшие количества фторида кальция, кремневой кислоты, фосфатов алюминия, железа и - редкоземельных элементов. В растворе находятся аммиачная селитра и моноаммоний-фосфат. Процесс нейтрализации протекает с выделением тепла. Температуру поддерживают на уровне 110 С. Непоглощенный аммиак улавливают из отходящего газа водой или азотной кислотой. При дальнейшей нейтрализации до рН 6 - 6 8 часть моноаммоний-фосфата превращается в диаммонийфосфат. [20]
Из азотнокислотной вытяжки, полученной разложением фосфата 5 % - ным избытком 50 - 53 % - ной азотной кислоты ( в расчете на СаО), после кристаллизации нитрата кальция при - 15 фильтрат содержит [24]: 18 - 21 % Р205, 5 5 - 6 5 % СаО, 4 5 - 5 5 % азота ( общ. [21]
Первый показатель является постоянным при использовании одного и того же вида сырья в сравниваемых вариантах, второй - зависит от концентрации и нормы азотной кислоты, температуры, при которой ведут процесс кристаллизации нитрата кальция. [22]
 |
Растворимость кремнефторида и фосфатов кальция в смесях фосфорной и азотной кислот. Изотерма 60 С. [23] |
Исследование пятикомпонентной системы СаО - Р208 - N206 - - CaSiF6 - Н20, аналогичное четверной системе СаО - Р205 - CaSiFe - - Н20, показало, что добавление кремнефторида кальция к четверной системе СаО - Р205 - N205 - Н20 [16, 17], так же как и к тройной системе СаО - Р208 - Н20 [1-6], смещает кривые совместного насыщения, поля кристаллизации и узловые точки: поле кристаллизации дикаль-цийфосфата расширяется, увеличивается также поле кристаллизации нитрата кальция, а поле кристаллизации монокальцийфосфата сужается со всех сторон. [24]
При разложении фосфатов одной азотной кислотой применяется политермическая кристаллизация нитрата кальция, основанная на уменьшении растворимости Ca ( NO3) 2 при понижении температуры. Кристаллизация нитрата кальция проводится по непрерывной схеме в системе поверхностных кристаллизаторов, охлаждаемых последовательно водой и охлаждающим рассолом до температуры минус 5 - 10 С. Осажденный нитрат кальция отфильтровывается, а азотно-фосфорнокислый раствор аммонизируется, выпаривается и гранулируется. При получении удобрения с содержанием калия к выпаренному раствору добавляется кристаллический хлористый калий. [25]
При азотнокислотном разложении фосфатов применяется политермичеокая кристаллизация нитрата кальция, основанная на уменьшении растворимости Са ( МОз) 2 при понижении температуры. Процесс кристаллизации нитрата кальция проводится по непрерывной схеме в системе поверхностных кристаллизаторов, охлаждаемых последовательно водой и охлаждающим рассолом. [26]
Цри разложении фосфорита Ка-ратау наибольшая степень выделения СаО соответствует 20 % - ному избытку HNO3 сверх стехиометри - ческой нормы и 55 % - ной концент - рации азотной кислоты. Процесс кристаллизации I нитрата кальция осуществляется по J непрерывной схеме в системе поверхностных кристаллизаторов, охлаждаемых последовательно водой и охлаждающим раствором. Разработан способ кристаллизации нитрата кальция с прямым отнятием тепла охлаждающей жидкостью, не смешивающейся с раствором. [27]
Температура начала кристаллизации нитрата кальция повышается с увеличением содержания его в растворе или, что то же, с увеличением концентрации используемой для приготовления вытяжки азотной кислоты. Чем выше температура начала кристаллизации нитрата кальция, тем больше повышается температура раствора в результате кристаллизации, вследствие большего количества образующейся твердой фазы. Взвешенные частицы шлама понижают стойкость пересыщенной системы и повышают вероятность образования зародышевых кристаллов. [28]
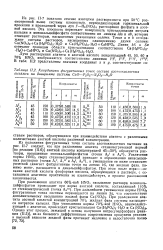 |
Координаты фигуративных точек состава азотнокислотных вытяжек на диаграмме системы СаО - P2Ob - N2O5 - H2O. [29] |
На рис. П-7 показано сечение изотермы растворимости при 50 С рассмотренной выше системы плоскостью, перпендикулярной горизонтальной проекции и проходящей через луч F - Н6 ( МО3) б растворения фосфата в азотной кислоте. Эта плоскость пересекает поверхность кристаллизации нитрата кальция и монокальцийфосфата соответственно по линиям Ida и аЬ, которые отвечают растворам, насыщенным указанными солями. [30]
Страницы: 1 2 3 4