Кристаллизация - соль
Cтраница 3
При кристаллизации соли охлаждением раствора осадок также отделяют от жидкости фильтрацией и определяют выход соли аналогично предыдущему. Опыт проводят с осуществлением или полного цикла разделения сильвинита, или полного цикла разделения насыщенного раствора солей или отдельных элементов одного и другого циклов. [31]
Для кристаллизации солей из водных растворов применяются различные способы создания условий пересыщения раствора. Испарение воды может производиться интенсивным способом при кипении раствора в выпарном аппарате и экстенсивным путем при медленном поверхностном испарении. [32]
Обычно кристаллизация соли начинается сразу же при сливании эквимолекулярных количеств реагентов в спирте или этиланетате. После разбавления эфиром соль отделяют и промывают эфиром. [33]
При кристаллизации одновалентной соли из ненасыщенных растворов двухвалентной соли, по Странскому, смешанные кристаллы вообще не могут образоваться, и в этом он видит причину отрицательных результатов в опытах Хлопина и Никитина. Гримм [7] совершенно ошибочно считает, что представление Странекого о структуре смешанных кристаллов нового рода близко к представлению Хлопина и Никитина. На самом деле они противоположны. Действительно, по Странскому, при перекристаллизации первоначально выпавших кристаллов должны образоваться большие кристаллы соли, построенной из двухвалентных ионов, на поверхности которых будет находиться одноионный слой соли, построенный из одновалентных ионов. Этот слой легко может быть удален простым промыванием. Иными словами, по Странскому, смешанные кристаллы нового рода вообще не могут существовать. [34]
Изучение кристаллизации солей из содержащих примеси растворов представляет значительный интерес, который обусловлен широким распространением этого процесса в различных областях промышленности. Оно ведется в ряде направлений, одним из которых является выяснение закономерностей сокристаллизации примесей с основным веществом. В этой области выполнено большое количество работ f1 10 и др. ], связанных в основном с проблемой получения чистых веществ. [35]
Механизм кристаллизации солей обратен механизму их растворения. При высокой концентрации ионов в рассоле плотность гидратной оболочки молекул воды снижается, уменьшается их разрывное действие и при насыщении рассола ионы солей соединяются в кристалл. Попадание вновь образованного кристалла соли ( кирпичика накипи) в кладку образующейся накипи или в состав частицы шлама предопределяется его расстоянием ( а следовательно, силой притяжения) в момент образования до ближайшего из этих двух возможных центров кристаллизации. Таким образом, образуется либо твердая накипь на поверхностях нагрева, либо шлам в граничном слое, выносимый затем в объем всего кипящего рассола. [36]
Процесс кристаллизации солей изучается с помощью биологического микроскопа ( фиг. [37]
Кинетика кристаллизации солей из пересыщенных растворов определяется процессами пересыщения, образования зародышей и роста кристаллов. Она такяе в известной мере зависит от образования сростков и дробления кристаллов в результате столкновения их между собой и со стенками кристаллизатора. Кроме того, кассовая кристаллизация имеет некоторые особенности. В отличие от роста монокристаллов, происходящего обычно при небольших пересыщениях, в условиях массовой кристаллизации рост кристаллов происходит в более широкок диапазоне изменения пересыщений и при интенсивном перемешивании раствора. Рост кристаллов в реальных растворах определяется не только пересыщением и гидродинамикой процесса, но зависит и от химического состава жидкой фазы. [38]
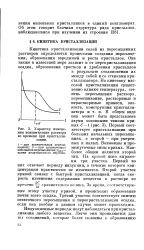 |
Характер изменения концентрации раствора во времени при кристаллизации. [39] |
Кинетика кристаллизации солей из пересыщенных растворов определяется процессами создания пересыщения, образования зародышей и роста кристаллов. [40]
Тепло кристаллизации соли и тепло, вносимое плавом, согласно тепловому балансу ( табл. 15) составляют соответственно 613 460 и 1 165 500 ккал. [41]
Скорость кристаллизации солей из растворов или расплавов характеризуется графиком, аналогичным представленному на рис. 1 - 6 [ 39, с. Как и всякий процесс фазового перехода кристаллизация может быть разделена на 3 стадии: I - инкубационный период, в течение которого происходит образование зародышей кристаллов; II - период интенсивного роста кристаллов; III - период старения, когда суммарная масса кристаллов и концентрация маточного раствора не изменяются, но происходит растворение мелких частиц и увеличение крупных, протекают процессы кристаллизации аморфных глобул, идет перераспределение дефектов кристаллов. [42]
 |
Клинографическое проектирование изотермы взаимной пары. [43] |
Поля кристаллизации солей ВХ, BY, CY и СХ ( в простейшем случае, когда компоненты системы не взаимодействуют между собой) обозначены проекциями поверхностей ( BX) peiEie, ( BY) pe2E2ei, ( CY) pe3E2e2 и ( CX) pe4EiE2e3 соответственно. [44]
Кинетика кристаллизации солей лз перескщеюшх растворов определяется ароцессак. Она такие в известной мере зависит от образования сростков к дробления кристаллов в результате столкновения их между ссбо: 1 и со стенкшли кристаллизатора. Крдае того, кассовая кристаллизация имеет некоторые особенности. В отличие от роста монокристаллов, происходящего обычно при небольших пере-снщениях, в условиях нассовой криста; глзации рост кристаллов происходит к более широком диапазоне измененир перосшценик и прг; интенсивном перемешивании раствора. Рост кристаллов з реальных раст - BODSX определяется не только пераснщением и гздродинашкой процесса, но зависит и от химического состава жидкой фазн. [45]
Страницы: 1 2 3 4