Сопряженный атом
Cтраница 2
Несопряженные атомы водорода ацетилена дают линии резонанса, соответствующие химическим сдвигам 2 45 - 2 65 млн 1 от носительно линии ТМС, а сопряженные атомы водорода - линии, соответствующие химическим сдвигам 2 8 - 3 1 млн-1 относительно линии ТМС. Эта область спектра заключена между линиями протонного резонанса алкана и алкена; линии протонного резонанса метилена и метина также находятся в этой области, что является ограничением данного метода. Если в молекуле производного ацетилена имеется ряд метиленовых и метановых групп, то линии протонного резонанса могут перекрывать друг друга, однако для идентификации можно использовать значение константы взаимодействия и различные растворители. Методом ЯМР можно прослеживать восстановление ацетилена до алкена и далее до насыщения и определять тип анализируемого ацетилена. [16]
Несопряженные атомы водорода ацетилена дают линии резо нанса, соответствующие химическим сдвигам 2 45 - 2 65 млн 1 от носительно линии ТМС, а сопряженные атомы водорода - линии, соответствующие химическим сдвигам 2 8 - 3 1 млн-1 относительно линии ТМС. Эта область спектра заключена между линиями протонного резонанса алкана и алкена; линии протонного резонанса метилена и метина также находятся в этой области, что является ограничением данного метода. Если в молекуле производного ацетилена имеется ряд метиленовых и метановых групп, то линии протонного резонанса могут перекрывать друг друга, однако для идентификации можно использовать значение константы взаимодействия и различные растворители. Методом ЯМР можно прослеживать восстановление ацетилена до алкена и далее до насыщения и определять тип анализируемого ацетилена. [17]
На первый взгляд кажется, что образование монолитного соединения двух одинаковых монокристаллов с идеально гладкими и чистыми поверхностями возможно при любой температуре и без приложения внешней энергии. Тогда между сопряженными атомами возникнут связи, граница раздела А ( рис. 1.1) исчезнет и произойдет сварка. Такой процесс кажется вероятным и не противоречит второму началу термодинамики, так как свободная энергия системы при этом должна уменьшиться на величину энергии двух исчезнувших поверхностей раздела. [19]
В таких ароматических системах сопряженные атомы связаны it - связями, образованными электронами, занимающими делокализованные it - орбиты. Легко можно показать, что такие электроны должны быть в состоянии образовать дативные связи с подходящим акцептором, подобно неподеленным парам электронов в таких молекулах, как аммиак и вода. [20]
Если нас интересует только разница в энергиях це-жду этими двумя системами, члены, содержащие Wc, компенсируются. Это упрощение обусловлено, конечно, тем, что все сопряженные атомы в рассматриваемой молекуле одинаковы; при наличии в молекуле гетероатомов члены W приходится сохранять ( см. гл. [21]
Верхние состояния каждой пары переходов являются вырожденными, если круговая траектория имеет постоянный потенциал. В циклических полиенах, содержащих ( 4 / 2) сопряженных атомов углерода, существует альтернирующий потенциал, обусловленный атомными ядрами. Поэтому вырождение запрещенной пары переходов снимается, давая нйзкоэнергетическое верхнее состояние с ( 2 / 1) узловыми плоскостями, проходящими через атомы и высокоэнергетическое верхнее состояние с ( 2 / 1) узловыми плоскостями, проходящими через середины связей. Это - верхние состояния переходов, дающие, соответственно, а - и р-полосы в спектрах поглощения. [22]
Движущей силой цикла Кальвина-Бенсона являются световые реакции. Солнечный свет поглощается молекулами хлорофилла ( см. рис. 20 - 21), в которых имеется кольцо сопряженных атомов углерода с делокализо-ванными электронами, окружающее атом магния. Молекула хлорофилла одного типа расположена в фотоцентре, или в ловушке, где и осуществляется химическая реакция, а другие хлорофиллы и родственные сопряженные молекулы окружают фотоцентр и играют роль антенн, поглощающих фотоны света и передающих электронное возбуждение к молекулам фотоцентра. [23]
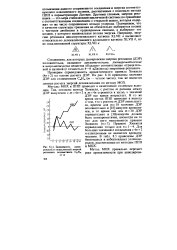 |
Зависимость дьюа. [24] |
Другими словами, энергия резонанса - это мера стабилизации циклической системы по сравнению с соответствующим соединением с открытой цепью, которая содержит то же число сопряженных атомов углерода. Подчеркнем, что в качестве структуры сравнения не обязательно выбирается полиен с чистыми двойными и ординарными связями, а выбирают тот полиен, у которого минимальная полная энергия. [25]
Согласно Дьюару, энергия резонанса равна разности энергии образования данного сопряженного соединения и энергии соответствующего классического пслиена. Другими словами, энергия резонанса - это мера стабилизации циклической системы по сравнению с соответствующим соединением с открытой цепью, которая содержит то же число сопряженных атомов углерода. Подчеркнем, что в качестве структуры сравнения не обязательно выбирается полиен с чистыми двойными и ординарными связями, а выбирается тот полиен, у которого минимальная полная энергия. [26]
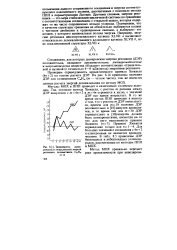 |
Зависимость дьюа. [27] |
Другими словами, энергия резонанса - это мера стабилизации циклической системы по сравнению с соответствующим соединением с открытой цепью, которая содержит то же число сопряженных атомов углерода. Подчеркнем, что в качестве структуры сравнения не обязательно выбирается полиен с чистыми двойными и ординарными связями, а выбирают тот полиен, у которого минимальная полная энергия. [28]
Верхняя я - орби-таль имеет еще одну нодальную плоскость, перпендикулярную направлению связи, поэтому является орбиталью антисвязываю-щего характера, хотя этот характер в данном случае выражен довольно слабо. В случае сопряженных двойных связей низ шая я-орбиталь основного состояния имеет ту же форму, что га для этилена, но плотность заряда распределяется по всей системе сопряженных атомов углерода, разность энергий я - и я - орбиталей меньше и первая полоса поглощения лежит при больших длинах волн. Если я - я-переходы не запрещены по симметрии, они весьма интенсивны ( емакс обычно от 104 до Ю6), и в отсутствие синглет-синглетных переходов с более низкой энергией часто именно они обусловливают флуоресценцию. [29]
Нас интересует одно специфическое применение метода ССП для открытых оболочек - его применение в рамках приближения Хюккеля для сопряженных радикалов, которые содержат неспаренные зт-электроны. В этом случае а-связи, как обычно, считаются локализованными; уравнения Рутана используются только для вычисления я - МО, так что АО базисного набора представляют собой набор р - АО сопряженных атомов. Как и для систем такого типа с закрытой оболочкой, если необходимо получать результаты с точностью, достаточной для химических целей, приходится использовать какую-то полуэмпирическую процедуру. Полезно попробовать применить приближение Поп-ла, оказавшееся таким удачным для сопряженных углеводородов с закрытой оболочкой. Уравнения Попла для систем с открытой оболочкой можно вывести из уравнений Рутана совершенно так же, как это было сделано для систем с закрытой оболочкой. [30]
Страницы: 1 2 3
