Аминокислота - содержонок
Cтраница 2
Титрование любой единичной ионизируемой группы аминокислоты дает кривую того же типа, что и кривая на рис. 4.3. Однако все аминокислоты содержат по крайней мере две диссоциирующие группы, а именно ос-амино ( или имино) - группу и а-карбоксильную группу. Кривая титрования, соответствующая диссоциации этих двух групп, приведена на рис. 4.8. В случае глицина два значения рК а отстоят сравнительно далеко друг от друга, и участки крутого подъема кривой четко отделяются один от другого. [16]
Синтез полиамидов путем полнконденсации аминокислот при повышенных температурах ( опыт 4 - 08) возможен лишь в том случае, если аминокислоты содержат более четырех метиленовых групп между амино - и карбоксильной группами. [17]
С помощью этих методов было выделено около 28 различных аминокислот. Все аминокислоты содержат по крайней мере две, а очень часто - три и более функциональные группы, в результате чего могут образовываться разветвленные макромолекулы и пространственные структуры. В табл. 28 приведено содержание важнейших аминокислот в некоторых часто встречающихся белках. Литературные данные о составе белков резко отличаются друг от друга, поэтому приводятся округленные цифры, позволяющие в общих чертах установить связь между свойствами полимера и составом элементарного звена. [18]
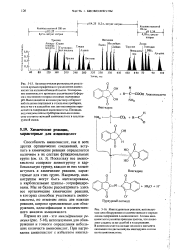
Способность аминокислот, как и всех других органических соединений, вступать в химические реакции определяется наличием в их составе функциональных групп ( см. гл. Поскольку все аминокислоты содержат аминогруппу и карбоксильную группу, каждая из них может вступать в химические реакции, характерные для этих групп. Например, аминогруппы могут быть ацетшшрованы, а карбоксильные группы - этерифициро-ваны. Мы не будем рассматривать здесь все органические химические реакции, в которых способны участвовать аминокислоты, но отметим лишь две важные реакции, широко применяемые для обнаружения, идентификации и количественного анализа аминокислот. [20]
 |
График к опреде - числить молекулярную массу лению молекулярной массы полимера. Это делают графи-осмотическим методом чески. Формулу ( 2 преобра. [21] |
Заряд на макромолекулах белка в водных растворах возникает обычно в результате диссоциации ионогенных групп. Белковые молекулы как продукты конденсации аминокислот содержат основные группы NH2 и кислотные СООН. [22]
 |
График к опреде - числить молекулярную массу. [23] |
Заряд на макромолекулах белка в водных растворах возникает обычно в результате диссоциадии ионогенных групп. Белковые молекулы как продукты конденсации аминокислот содержат основные группы NH2 и кислотные СООН. [24]
 |
График к определс - тический метод определения молеку. [25] |
Заряд на макромолекулах белка в водных растворах возникает обычно в результате диссоциации ионогенных групп. Белковые молекулы как продукты конденсации аминокислот содержат основные группы NH2 и кислотные СООН. [26]
Многие из них хорошо растворимы в воде. Это связано с тем, что аминокислоты содержат одновременно карбоксильную группу, обладающую кислыми свойствами, и аминогруппу, характеризующуюся основными свойствами. Поэтому аминокислоты способны образовывать соли как с кислотами, так и с основаниями, являясь, таким образом, амфотерными соединениями. [27]
Макромолекулы белков построены в основном из остатков а-аминокислот. Строение аминокислот схематически можно изобразить так: H2N - R-СООН, где R - углеводородный радикал. Некоторые аминокислоты содержат по одной группе - СООН и - МНз, - другие имеют две группы - СООН и одну - NH2, у третьих есть две группы - NH2 и одна группа - СООН. [28]
Первой стадией анализа белка является гидролиз, предпочтительно кислотный, хотя используют также протеолитический и щелочной гидролиз. Полученный элюат выпаривают досуха и обрабатывают с тем, чтобы 1) получить летучие производные аминокислот; 2) блокировать функциональные группы, осложняющие проведение анализа; 3) повысить чувствительность обнаружения. Поскольку белковые аминокислоты содержат разнообразные функциональные группы, в том числе карбоксильные, аминные, алифатические и ароматические гидроксильные, гуанидиновые, индольную и имидизоловую, решить все эти задачи достаточно сложно. Авторы работы [114] считают, что целесообразнее всего проводить N - ( О, 5) - три-метилсилилование аминокислот. В работе [115] отмечается, что аминокислоты несколько различаются по способности к образованию производных. Обычно сначала проводят этерификацию, а после этого М - ацилирование, хотя, по данным авторов работы [116], получение производных можно осуществить в одну стадию. [29]
Аминокислоты представляют собой бесцветные кристаллические вещества. Многие из них растворимы в воде. Ряд аминокислот содержат асимметрические атомы углерода и вращают плоскость поляризованного света. [30]
Страницы: 1 2 3