Соответствующая аминокислота
Cтраница 2
Синтез соответствующего фермента понижается или повышается в зависимости от концентрации соответствующей аминокислоты, но не путем обратной связи, т.е. путем блокирования соответствующего фермента, а путем изменения в активности гена, кодирующего соответствующий фермент. [16]
Обозначения: в случае моно - ДНФ-про-изводных приводится только символ соответствующей аминокислоты ( см. табл. 103), ди - ди - ДНФ-производные, ОН - 2 4-динитрофенол, NH2 - 2 4-динитро-анилин. [18]
Первый этап реакции пореаминирования заключается в вытеснении е-амино-групны лизина аминогруппой соответствующей аминокислоты. Образующееся шиффово основание субстрата с пиридоксальфосфатом таутомеризуется; в результате гидролиза освобождается соответствующая кетокпслота и протеид пиридоксаминфосфата, к-рый, в случае аспартат - и аланин-аминотрансфераз, имеет независимо от рН максимум поглощения при 330 ммк. L-аспарагина и L-глутамииа на различные a - кетокислоты. [19]
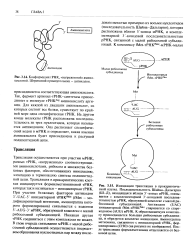
Трансляция осуществляется при участии мРНК, разных тРНК, нагруженных соответствующими аминокислотами, рибосом и множества белковых факторов, обеспечивающих инициацию, элонгацию и терминацию синтеза полипептидной цепи. При участии белковых факторов антикодон 3 - UAC-5 инициаторной тРНКШе1 ( fMet - модифицированный метионин, аминогруппа которого форматирована) связывается с кодовом 5 - AUG-3 мРНК, образующей комплекс с малой рибосомной субъединицей. Никакая другая тРНК соединиться с этим комплексом не может. [21]
С-О, относятся аминоацил-т РНК-син-тетазы, катализирующие ацилирование транспортных РНК соответствующими аминокислотами. [22]
Среды для определения валина, лейцина или изолейцина готовят без добавления соответствующей аминокислоты. [23]
Синтез N-защищенных кислот осуществляют обычным способом из n - хлоркарбобензоксихлорида и соответствующей аминокислоты в водно-щелочном растворе. В случае n - хлоркарбобензоксиаспарагина в качестве основания используют карбонат натрия, а соответствующее производное аспарагиновой кислоты получают с окисью магния. [24]
Синтез N-защищенных кислот осуществляют обычным способом из n - хлоркарбобензоксихлорида и соответствующей аминокислоты в водно-щелочном растворе. В случае и-хлоркарбобензоксиаспарагина в качестве основания используют карбонат натрия, а соответствующее производное аспарагиновой кислоты получают с окисью магния. [25]
Вместе с тем нельзя исключить и такую возможность как окисление аминоальдегида до соответствующей аминокислоты с последующим замыканием цикла в оксигидрастинин. [26]
Соединения GoGl3 и СоАп3 получаются при взаимодействии окиси кобальта с водным раствором соответствующей аминокислоты при нагревании. В частности, из вишнево-красного раствора, образующегося при нагревании окиси кобальта с раствором глицина, выделяются две соли, различающиеся по окраске и по содержанию кристаллизационной воды. [27]
Соединения CoGl3 и СоАп3 получаются при взаимодействии окиси кобальта с водным раствором соответствующей аминокислоты при нагревании. В частности, из вишнево-красного раствора, образующегося при нагревании окиси кобальта с раствором глицина, выделяются две соли, различающиеся по окраске и по содержанию кристаллизационной воды. [28]
Поставленные нами опыты показали, что при конденсации опиановой кислоты образуется смесь из соответствующей аминокислоты и меконил-уксусной кислоты; образования же - этилового эфира нами установлено не было. [29]
Для повышения селективности можно выбрать ауксотрофные мутанты, которые сами не приспособлены для синтеза соответствующей аминокислоты и используют аминокислоту, получаемую в побочном синтезе прежде всего при синтезе пептида. Сначала этот метод ограничивался в основном только ферментами бактерий, так как только бактерии могут выращиваться в больших объемах. Для того чтобы распространить этот метод на высокоорганизованные системы, можно было бы в принципе отклониться от метода, использующего культуры соответствующих клеток, поскольку этот метод сопряжен с большими затратами, и соответственно практическая ценность его невелика. [30]
Страницы: 1 2 3 4