Микробная культура
Cтраница 1
Микробная культура, пересеянная на свежую питательную среду, развиваясь, проходит несколько этапов роста. Начальный этап - стадия покоя, когда в течение некоторого времени микробные клетки не размножаются. Затем следует стадия бурного обмена веществ и размножения. [1]
Суточную микробную культуру на мясо-пептонном агаре смывают физраствором с таким расчетом, чтобы получить суспензию концентрацией 15 - 20 млрд, микробных клеток. Данную суспензию сохраняют на холоду при 4 - 8 в течение двух - трех месяцев и по мере надобности используют. [2]
Результат воздействия микробной культуры на ароматические углеводороды с длинной алифатической цепочкой определяется тем, способен ли данный микроорганизм разлагать бензойную, фенилуксусную или фенилакриловую кислоты. По наблюдениям фенилуксусная кислота более устойчива к действию микроорганизмов, чем бензойная, поэтому углеводороды с четным числом С-атомов в боковой цепи в результате последовательного отщепления двууглсродных фрагментов в процессе р-окислешш обычно трансформируются в фенилуксус. Углеводороды с нечетным числом атомов углерода в алифатической цепочке часто ассимилируют полностью, так как образующаяся в процессе ( 3-окисления бензойная кислота разлагается некоторыми культурами. [3]
При внесении микробной культуры в питательную среду клетки вступают в лаг-фазу /, которая может быть названа также фазой приспособления. Продолжительность этой фазы зависит, в частности, от адаптированности микроорганизмов к органическим веществам, содержащимся в среде. [4]
Для серологической идентификации неизвестной микробной культуры в лаборатории должна быть соответствующая агглютинирующая сыворотка. [5]
На рост и биосинтез микробных культур влияют также различные ядовитые вещества. [6]
Чем отличаются цикл развития микробной культуры и клеточный цикл. [7]
Всестороннее изучение характера роста микробных культур является одним из главнейших методов микробиологического исследования. В основе роста популяции микроорганизов, как совокупности особей, обитающих, в одном ареале ( при проведении культивирования в аппарате), лежат процессы роста, размножения ( деления) и отмирания отдельных микроорганизмов. Хотя кинетика роста популяции не сводима к кинетике роста отдельных микроорганизмов, но так как закономерности низшего уровня ( в данном случае клеточного) сохраняют определенную автономность на высшем ( популяционном) и только преобразуются при усложнении биосистемы, то представляется целесообразным рассмотреть общие положения процесса роста микроорганизмов, которые в какой-то мере могут объяснить особенности поведения популяции. [8]
Большую роль в развитии микробной культуры играет концентрация углеводородов, которая для жидких и твердых углеводородов, диспергированных в воде, зависит от поверхности контактирования с водой. При встряхивании культур концентрация их в среде значительно возрастает. Труднорастворимые углеводороды могут быть окислены только на поверхности, граничащей с водой. У легкорастворимых углеводородов, например у низших алифатических и ароматических соединений, имеются оптимальные и токсические концентрации; в последнем случае микроорганизмы растут только на определенном расстоянии от углеводорода. К токсическим веществам, потребляемым микроорганизмами в невысоких концентрациях, относятся нафтеновые кислоты, которые содержатся в нефти. [9]
РА на стекле с различными микробными культурами или их полными АГ, взятыми в последовательно уменьшающихся разведениях. Для изучения активности цветных антител определяют их микробный титр. За микробный титр цветных антител принимается та минимальная концентрация гомологичных микробных клеток в 1 мл взвеси, капля которой вызывает еще выраженную агглютинацию цветных антител на предметном стекле в течение 5 мин. Специфичность РЦА устанавливают в опытах с гетерологич-ными микробными культурами и их смесями. С гетеро-логичными видами микробов и даже с R-формами их цветные антитела не должны давать неспецифических реакций. Препараты цветных антител хорошо сохраняются при 4 - 8 без добавления консерванта, роль которого выполняет бриллиантовая зелень, весьма прочно-соединяющаяся с частицами целлюлозы. Кроме того, цветные антитела могут подвергаться замораживанию и длительно храниться в таком состоянии, не снижая своей активности. В этом их большое преимущество перед угольными, ализариновыми антителами, а также перед антительными эритроцитами, которые при замораживании, как правило, повреждаются. [10]
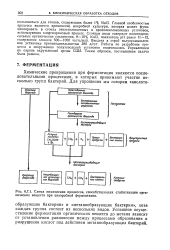 |
Схема химических процессов, способствующих стабилизации органических веществ при анаэробной ферментации. [11] |
Главной особенностью процесса является применение микробной культуры, которая может функционировать в стоках этиленгликолевых и пропиленгликолевых установок, использующих хлоргидриновый процесс. Сточные воды содержат полигидрок-сильные органические соединения, 8 - 10 % NaCl, показатель рН равен 11 - 12, содержание гликоля 500 - 1000 часть / млн. Введена в строй полупромышленная установка производительностью 380 л / сут. [12]
Отсюда очевидно, что ферменты могут находиться в солоде, микробных культурах и ферментных препаратах из них в различных количествах и обладать неодинаковой активностью. [13]
 |
Автолитические процессы при росте и делении клеток. [14] |
Роль автолитических ферментов во множественных физиологических процессах на всем протяжении развития микробной культуры очень велика. [15]
Страницы: 1 2 3 4