Различные аминокислота
Cтраница 1
Различные аминокислоты удобнее разбирать, разбив их на группы таким образом, что представители каждой группы или групп имеют общее происхождение, или могут превращаться друг в друга. [1]
Различные аминокислоты могут дезаминироваться неодинаковыми путями, и дезаминирование одной определенной аминокислоты может осуществляться при помощи нескольких механизмов. Кроме того, существуют значительные видовые различия в преобладании того или другого механизма дезаминирования. Несмотря на указанные различия, дезаминирование большинства аминокислот осуществляется у самых разнообразных видов в основном двумя общими путями, а именно: путем окислительного дезаминирования ( стр. [2]
Различные аминокислоты используются организмом в нормальных или патологических условиях для того, чтобы связывать другие вещества. То же самое соединение обнаруживается в моче людей, получавших с пищей бензойную кислоту или вещества, которые могут в нее превращаться. [3]
Различные аминокислоты, выделенные из белков, были синтезированы уже давно, главным образом с целью установления или подтверждения строения. [4]
Вводя различные аминокислоты и изменяя порядок их введения, можно синтезировать полипептиды, содержащие остатки различных аминокислот. Фишер синтезировал полипептид, состоявший из 18 аминокислотных остатков ( стр. [5]
Различные аминокислоты псно-лт зуются организмом в нормальных или патологических условиях для TOI O, чтобы связывать другие вещества. Так, моча лошадей постоянно содержит зпачп глчьные количества гип-п у р о в о и к и с л о т ы - бс нзоилгликоколя С ( ИЙСО-N11-СН2СООН. То же самое соединение обнаруживается в моче людей, получавших с пищей бензойную кислоту пли вещества, которые могут в нее превращаться. [6]
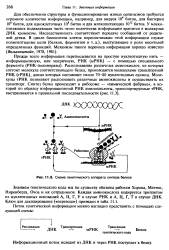 |
Схема генетического аппарата синтеза белков. [7] |
Распознавание различных аминокислот, из которых состоит молекула соответствующего белка, производится молекулами транспортной РНК ( тРНК), длина которых составляет около 70 - 80 нуклеотидных единиц. Молекулы тРНК позволяют распознавать различные аминокислоты и осуществлять их транспорт. [8]
Катаболизм различных аминокислот будет рассмотрен в гл. Здесь мы хотим подчеркнуть только следующее. [9]
Исследование различных аминокислот [177-182] показало, что в комплексах между металлами и ацетатными группами наблюдается главным образом ионная связь, а между металлами и аминогруппами - координационная. [10]
У различных аминокислот гидрофобные или гидрофильные свойства выражены сильнее или слабее в соответствии с химической природой радикалов, входящих в их состав. Гидрофобность или гидрофилыюсть пептидов определяется их аминокислотным составом. Поверхность глобул большинства нативных белков цитоплазмы в целом гидрофильна, так как остатки гидрофобных аминокислот спрятаны внутрь глобул. У белков мембран, наоборот, гидрофобные остатки аминокислот располагаются на поверхности. [11]
Чем больше различных аминокислот соединяется между собой, тем больше число возможных полипептидов. Многие белки построены из большего числа аминокислотных единиц. Кроме того, во многих белковых цепях некоторые аминокислоты повторяются. Так, например, из одного типичного белка с молекулярным весом 34 000 было выделено 12 различных аминокислот. [12]
Чем больше различных аминокислот соединяется между собой, тем больше число возможных полипептидов. [13]
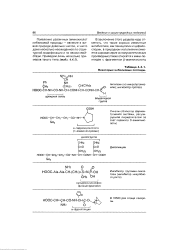 |
Некоторые небелковые пептиды. [14] |
Появление различных аминокислот небелковой природы - явление в живой природе довольно частое, и часто даже несколько неожиданное по структурной модификации и по своим свойствам. [15]
Страницы: 1 2 3 4