Природные аминокислота
Cтраница 3
Во-кторых, все природные аминокислоты ( за исключением гликоколла) оптически деятельны. При этом самым замечательным является тот факт, что все они имеют сходное пространственное расположение атомов. Аминокислоты, имеющие зеркальнопротивоположную конфигурацию атомов, не встречаются в нормальных живых клетках. Лишь при некоторых болезненных процессах, например в раковых клетках, появляются белки, состоящие из аминокислот с такой конфигурацией. [31]
Перед хроматографическим разделением природных аминокислот, чтобы предотвратить размывание задней границы пятен и ее деформацию, иногда приходится удалять мешающие анализу вещества. Это в особенности относится к пробам мочи и гидролизатов белков или пептидов, содержащих большие количества солей. [32]
Пролин и оксипролин - единственные природные аминокислоты, у которых аминогруппа является частью пир-ролидинового кольца. [33]
Стереохимические отношения в ряду природных аминокислот, входящих в состав белков, в настоящее время достаточно ясны. [34]
Стсреохпмпческпе отношения в пялу природных аминокислот, входящих в состав белков, в настоящее время достаточно ясны. [35]
Настоящая глава посвящена рассмотрению природных аминокислот. Из них первыми стали известны аспарагин, открытый в 1806 г., и цистин, открытый в 1810 г. Начиная с этого времени было обнаружено существование более 80 аминокислот. Кривая, изображенная на фиг. Вместе с тем после 1935 г., в котором был открыт треонин, не найдено ни одной новой аминокислоты, входящей в состав белков, что видно из сплошной кривой, также изображенной на фиг. Аминокислоты, обычно обнаруживаемые в белковых гидролизатах, рассматриваются в следующем разделе. Те аминокислоты, которые редко встречаются в белках, и аминокислоты, найденные в составе соединений других типов или в свободном состоянии, обсуждаются в последних разделах настоящей главы. [36]
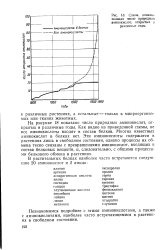 |
Схема, показывающая число природных аминокислот, открытых в различные годы. [37] |
На рисунке 18 показано число природных аминокислот, открытых в различные годы. Как видно из приведенной схемы, не все аминокислоты входят в состав белков. [38]
Знак эффекта Коттона у всех исследованных производных природных аминокислот L-конфигурации положителен. [39]
Как вы увидите ниже, все природные аминокислоты ( за исключением глицина) имеют по крайней мере один хиральный центр. Установление конфигурации - углеродного атома показало, что все они имеют S-кон-фигурацию. [40]
Двумерным хроматографированием удается разделить почти все природные аминокислоты. При этом способе через хроматографиче-скую бумагу пропускают два растворителя в двух взаимно перпендикулярных направлениях. [41]
К настоящему времени известно около 200 природных аминокислот. [42]
Ниже представлены правильные абсолютные конфигурации этих природных аминокислот. [43]
В настоящее время известно около 180 различных природных аминокислот. [44]
В настоящее время известно около 180 различных природных аминокислот. Особенно много аминокислот выделено за последние годы после того, как благодаря развитию методов очистки и успехам аминокислотного анализа были предприняты систематические исследования животного и растительного материала. [45]
Страницы: 1 2 3 4