Молекулярная диаграмма
Cтраница 2
Из приведенных молекулярных диаграмм можно сделать вывод, что при элек-трофильном замещении в анилине атака будет в основном направлена на о - и я-уг-леродные атомы, тогда в нитробензоле следует преимущественно ждать образования л-изомера. В этих случаях эксперимент находится в полном согласии с выводами теории. [16]
На молекулярной диаграмме приведены порядки л-связей и дробные заряды на атомах. Безусловно, расчеты этих величин являются сугубо приближенными, однако они правильно отражают относительное распределение ( 5) - зарядов на а -, ( 3 - и у-атомах углерода. [17]
В молекулярных диаграммах индекс свободной валентности указывается при стрелках, проведенных от данного атома. [18]
На молекулярных диаграммах, как это и сделано, указывают обычно заряды на атомах и порядки связей лишь для одного из эквивалентных атомов и одной из эквивалентных пар атомов. [19]
Особенно полезны молекулярные диаграммы для сложных би - и полициклических соединений. Выше приведена диаграмма для азулена. Поэтому реакции электрофильного замещения ( нитрование, сульфирование, галогенирование и др.) легко проходят в пятичленном цикле и не идут в семичленном. [20]
Ниже приводится молекулярная диаграмма 1 3-бутадиена. [21]
Вводятся также молекулярные диаграммы индексов. Индексы связей и атомов определяются, однако, прежним путем - методом мезомерии, но теперь индексы связей численно равны половине прежних электронных зарядов связей. Предполагается, что они представляют собой долю пары я-электронов, участвующих в образовании данной связи, и близки ( s apparentent) по смыслу к характеру двоесвязности Полинга и порядку связи по Коулсону ( см. стр. Индексы связи, или, иначе, индексы я-связи, указывают, в какой степени рассматриваемая связь ведет себя как двойная [ там же, стр. Для индексов атомов, численно равных теперь прежним электронным зарядам атомов, предлагается также название индексы свободной валентности, чтобы подчеркнуть аналогию с числами свободной валентности Коулсона. [22]
Направления использования молекулярных диаграмм перечислены ниже. [23]
 |
Уровни я-орбиталей бутадиена и их заселение.| Распределение электронной плотности и узловые линии ороиталей бутадиена. [24] |
Обозначения на молекулярных диаграммах: 1) полный порядок связи ( указывается на связях между соседними атомами углерода) Р ( / с н Svp. О, 1, 2 - число образующих я-связи электронов на дан ной МО OF); ptj ciCj - парциальный порядок связи - мера взаимодействия электронных облаков соседних атомов i и /, причем меньшие порядки связи соответствуют большим межатомным расстояниям; 2) индекс свободной валентности F 4 732 - - Р - ( изображен стрелкой с числом над. [25]
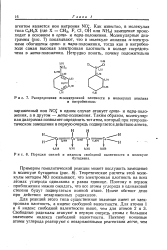 |
Распределение я-электронной плотности в молекулах анилина.| Порядки связей и индексы свободной валентности в молекуле. [26] |
Таким образом, молекулярная диаграмма позволяет определить тот атом, который при гетероли-тическом замещении в первую очередь подвергается действию агента. [27]
В этом отношении молекулярные диаграммы - электронный портрет молекулы - одновременно представляют собой правдоподобное изображение ее реакционной способности ( une veritable image de sa reactivite) [ там же, стр. Такие формулы должны помочь в предвидении, по крайней мере в главных чертах, химического поведения молекулы с такой точностью и полнотой, с какой никакая другая формула этого сделать не может. Примерно так пишет Пюльман в своем обзоре. [28]
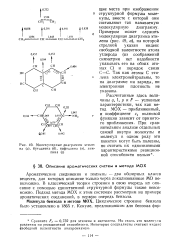 |
Молекулярные диаграммы этилена ( а, бутадиена ( б, нафталина ( в, анилина ( г. [29] |
Примером может служить молекулярная диаграмма этилена ( рис. 49, а), на которой стрелкой указан индекс свободной валентности атома углерода ( из соображений симметрии нет надобности указывать его на обоих атомах С) и порядок связи С-С. Так как атомы С этилена электронейтральны, то на диаграмме ни заряды, ни электронная плотность не указаны. [30]
Страницы: 1 2 3 4