Ацеталея
Cтраница 1
Выходы ацеталеи ( или альдегидов, если реакционная смесь подвергается гидролизу без выделения ацеталя) зависят до известной степени от строения реагента Грипьяра, однако наиболее важным фактором являются условия реакции и обработка образующейся реакционной смеси. Детальный ход реакции не изучен, но качественные наблюдения позволяют прийти к заключению о том, что процесс протекает сложно. Так, прибавление орто-эфира к эфирному раствору реагента Гриньяра с последующей обработкой смеси приводит к низким выходам ацеталеи. Выходы существенно повышаются, если перед обработкой смесь прокипятить в течение нескольких часов, и достигают максимальных, если провести отгонку эфира от реакционной смеси и осторожно нагреть остаток до начала бурной экзотермической реакции. Эти особенности реакции затрудняют применение ее в крупномасштабных синтезах. [1]
Для получения ацеталеи реакционную смесь обрабатывают водным раствором хлористого аммония или уксусной кислотой. Для получения альдегида реакционную смесь разлагают минеральными кислотами. [2]
В случае некоторых ацеталеи кетена две молекулы этиленового соединения могут реагировать как одна молекула диена. [3]
Такая реакция является общей для ацеталеи и ароматических соединений. Ацетальную молекулу активирует присутствие близ реакционного центра электропоакцепторных заместителей. [4]
 |
Свойства пленок из поливинилового спирта. [5] |
Наиболее интересен поливинилбутираль, так как из ацеталеи только он способен давать технические пленки. [6]
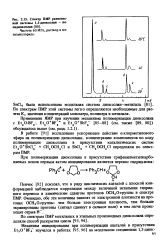 |
Спектр ПМР равновесной системы 1 3-диоксолан - по-лндиоксолан. [7] |
Пенчек [92] показал, что в ряду циклических ацеталеи с плоской кон-формацией наблюдается корреляция между величиной энтальпии гидрид-ного переноса и химическим сдвигом протонов ОСН20 - группы в спектре ПМР. [8]
Реакция Чичибабина - Бодру редко используется для синтеза насыщенных жирных и алициклических ацеталеи, поскольку такие ацетали выгоднее получать прямой ацетализацией. Для синтеза некоторых ацеталеи разветвленных или труднодоступных альдегидов метод все же был использован. [9]
На рис. 2 приведена зависимость степени гидрирования альдегидов, ацеталеи и сложных эфироз от продолжительности работы катализатора при температуре 200 С. [10]
Буато [4] взял патент на такой же процесс с целью получения ацеталеи. Рейхерт, Бэлей и Ньюлэнд [5] изучали получение ацеталеи из ацетилена и ряда одноатомных спиртов, с применением как катализатора сернокислой ртути с серной кислотой. [11]
 |
Условия гидролиза а р-непредельных и иолиеновых ацеталеи. [12] |
Поскольку этинильная группа обладает значительным - / - эффектом, скорость гидролиза ацеталеи с этинильной группой в а р-положении к ацетальной группе ниже скорости гидролиза этиленовых и насыщенных ацеталеи. Кроме того, ацетиленовые альдегиды, как правило, мало устойчивы в кислой среде, поэтому гидролиз ацетиленовых ацеталеи представляет большие методические трудности, чем гидролиз этиленовых ацеталеи. [13]
Отношение коэффициентов активности не зависит от состава среды, так как ионизованная форма ацеталеи и активированный комплекс одинаковы по заряду, составу и строению. Именно эта зависимость приводится в качестве основного аргумента в пользу того, что протонирование ацеталеи происходит по типу индикаторов Гамметта. В общем случае процессу гидролиза ацеталеи способствует параллельная ориентация связи - С-О - неспаренной пары электронов непротонированного кислорода. Для циклических ацеталеи такая ориентация затруднена и поэтому циклические аце-тали на несколько порядков менее реакционноспособны, чем линейные ацетали ( гл. Механизм кислотно-каталитического распада олигомеров лолиоксиметилена также описан в гл. [14]
Анализ результатов показал, что при повышении температуры до 250 С степень гидрирования ацеталеи и альдегидов ( кривые 1, 2) возрастает, при дальнейшем увеличении температуры до 280 С степень гидрирования альдегидов и ацеталеи практически постоянна. Степень гидрирования эфиров ( кривая 3) имеет оптимум при температурах 245 - 255 С. [15]
Страницы: 1 2 3 4