Ацеталея
Cтраница 2
Однако высшие гомологи пропаргилового альдегида, начиная с гептин-2 - аля образуются при гидролизе ацеталеи с выходами 55 - 92 %, что объясняется повышением устойчивости ацетиленовых альдегидов с ростом цепи. [16]
В то же время Л. А. Яновская полагает, что сильное влияние электронных факторов на реакционную способность ацеталеи в реакциях с виниловыми эфирами связано несомненно с механизмом этой реакции, который, по ее мнению, протекает как циклический электронный перенос с четырьмя центрами ( см. выше, стр. [17]
Рассмотренные выше факты, с одной стороны, свидетельствуют о достаточно высокой устойчивости активных центров полимеризации циклических ацеталеи, с другой стороны, - о том, что их реакционная способность отличается от реакционной способности активных центров полимеризации простых циклических эфиров. Предположительно им можно приписать структуру карбоксониевого иона. [18]
Научная новизна работы заключается в том, что впервые изучены продукты, кинетика и механизм взаимодействия ряда циклических ацеталеи с гипохло-ритом натрия и диоксидом хлора, определены активационные параметры процессов. Оценена относительная активность исследованных 1 3-диоксациклоалканов по отношению к гипохлориту натрия и диоксиду хлора. Показано, что процесс окисления можно интенсифицировать путем добавления в систему силикагеля или стабильных нитроксильных радикалов. Изучены продукты окисления амил ( 4-метилен - 1 3-диоксоланил) сульфида рядом окислителей. Установлено, что амил ( 4-метилен - 1 3-диоксоланил) сульфид проявляет бактерицидные свойства и подавляет рост сульфатвосстанавливающих бактерий. [19]
Как следует из приведенных данных, с увеличением срока работы катализатора с 12 до 53 ч степень гидрирования ацеталеи ( кривая /) падала с 70 до 40 %, альдегидов ( кривая 2) - с 73 до 31 %, а эфиров ( кривая 3) - с 55 до 20 % и дальше практически не менялась. [20]
Для получения простых эфиров вторичных и третичных спиртов из ортомуравьиного и соответственно ортоугольного эфира реакцию проводят в более жестких условиях, чем для получения ацеталеи. [21]
Поскольку этинильная группа обладает значительным - / - эффектом, скорость гидролиза ацеталеи с этинильной группой в а р-положении к ацетальной группе ниже скорости гидролиза этиленовых и насыщенных ацеталеи. Кроме того, ацетиленовые альдегиды, как правило, мало устойчивы в кислой среде, поэтому гидролиз ацетиленовых ацеталеи представляет большие методические трудности, чем гидролиз этиленовых ацеталеи. [22]
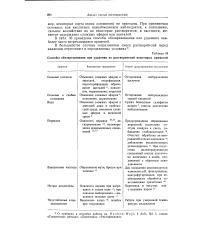 |
Способы обезвреживания или удаления из растворителей некоторых примесей. [23] |
При применении основных или кислотных ионообменников наблюдается, к сожалению, сильное воздействие их на некоторые растворители; в частности, меняется содержание сложных эфиров или ацеталеи. [24]
Правила Содержат требования безопасности при проектировании, строительстве и реконструкции в производствах формалина, уротропина, полистирола и сополимеров стирола, винилацетата, поливинилового спирта и его ацеталеи, сложных эфиров фталевой кислоты, аминопластов и меламина, слоистых пластиков и текстолита, феноло-формальдегидных смол и прессматериалов, эластичного пенополиуретана непрерывным способом. [25]
При применении основных или кислотных ионообменников наблюдается, к сожалению, сйль ное воздействие их на некоторые растворители; в частности, меняется содержание сложных эфиров или ацеталеи. [26]
Анализ результатов показал, что при повышении температуры до 250 С степень гидрирования ацеталеи и альдегидов ( кривые 1, 2) возрастает, при дальнейшем увеличении температуры до 280 С степень гидрирования альдегидов и ацеталеи практически постоянна. Степень гидрирования эфиров ( кривая 3) имеет оптимум при температурах 245 - 255 С. [27]
Несмотря на мягкие условия этих реакций выходы альдегидов невелики, что связано с их малой устойчивостью в этих условиях. Кроме ацеталеи исходными для получения альдегидов диаце-тиленового ряда могут служить и другие диацетиленовые производные. [28]
Реакция Чичибабина - Бодру редко используется для синтеза насыщенных жирных и алициклических ацеталеи, поскольку такие ацетали выгоднее получать прямой ацетализацией. Для синтеза некоторых ацеталеи разветвленных или труднодоступных альдегидов метод все же был использован. [29]
НАД) окисление спиртов и ацеталеи до альдегидов н кетонов. Состоит из двух ( печень лошади) или четырех ( дрожжи) одинаковых субъединиц с мол. [30]
Страницы: 1 2 3 4