Ацеталь
Cтраница 1
Ацетали и кетали могут содержать представляющие опасность пероксиды, подобные тем, которые часто содержатся в простых эфирах. Необходимо ознакомиться с обсуждением вопроса о таких пероксидах в разд. [1]
Ацетали, кетали, азины, гидразоны, семикарбазоны, имины размещены в таблице как производные соответствующих карбонильных соединений по функциональной группе и расположены следом за названием альдегида или кетона. [2]
Ацетали ( и кетали) являются диэфирами двухатомных спиртов ( ге. По своим химическим свойствам они существенно отличаются от полуацеталей и полукеталей. Как и простые эфиры, аце-тали не окисляются, не реагируют с восстановителями, устойчивы к действию оснований. Поэтому реакции ацетализации применяют для защиты карбонильной группы. [3]
Ацетали - бесцветные жидкости с приятным запахом; водными растворами кислот они быстро расщепляются на альдегид и спирт. Известны аналогичные соединения кетонов, но они получаются другим путем. [4]
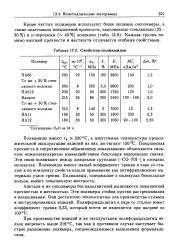 |
Свойства полиамидов. [5] |
Ацетали и их сополимеры без наполнителей выделяются повышенной прочностью и жесткостью. [6]
Ацетали и кетали получают также конденсацией ацетилена и его гомологов со спиртами или фенолами ( о поливинилацеталях см. стр. [7]
Ацеталь ( XIX) получен также обработке... [8]
Ацетали широко распространены в природе. Так, моносахариды существуют в виде внутренних полуацеталей, которые в зависимости от величины образовавшегося цикла называют пиранозами или фуранозами ( см. стр. [9]
Ацетали, полученные из ( 89), позволяют избежать неудобств, связанных с образованием диастереомеров ( ср. Исключительная лабильность ацеталей ацетона [ из ( 91) ] приводит к тому, что их используют только при решении специальных задач, тогда как ацетали ацетальдегида [ из ( 90) ] находят применение в стандартном методе [143] установления положения О-ацильных групп в полисахаридах путем негативной метки свободных гидроксильных групп. Эффектная стадия замещения мето-ксильной группы в таких ацеталях на ( З - метоксиэтоксильную [359] дает производные, для которых характерна необычная чувствительность к расщеплению под действием кислот Льюиса ( ZnCl2 или TiCU) в СН2С12 при комнатной температуре или ниже нее, однако они остаются устойчивыми к действию оснований, мягкой кислотной обработке и действию многих реагентов, используемых для удаления ряда других защитных групп. К значительным преимуществам метода следует отнести также применимость не только ко вторичным и первичным, но и к третичным гидроксильным группам, а также возможность выбора пути синтеза: реакция хлорэфира ( 148) с алкоксидом в ТГФ или глиме при 0 С или со спиртом и Mso - Pr2EtN в СН2С12 при 25 С и реакция аммонийной соли ( 149) со спиртом в MeCN при кипячении. [10]
Ацетали получают с помощью эфиров Ортокремневои кислоты следующим обр зом [736]: смешивают 1 моль альдегида или кетона с 2 - 3 молъ соответствующего 6ej водного спирта и 1 1 моль эфира артокроыиевои кислоты и добавляют 10 капель ET. J сыщенного при комнатной температуре спиртового раствора IIC1 или пропуска несколько пузырьков сухого НСГ. [11]
Ацетали являются устойчивыми соединениями и могут быть выделены после нейтрализации реакционной смеси. Ключевым интермедиа-том в этой реакции служит стабилизованный кислородом катион ( 23), образующийся при отщеплении воды от протонированной формы полуацеталя. [12]
Ацетали, кетали, азины, гидразоны, семикарбазоны, имины размещены в таблице как производные соответствующих карбонильных соединений по функциональной группе и расположены следом за названием альдегида или кетона. [13]
Ацетали являются гел-диэфирами, но, в отличие от соответствующих геж-диолов, они могут быть получены в чистом виде и представляют собой жидкости, которые можно очищать перегонкой. Образование ацеталей является обратимым процессом, и ацетали легко гидроли-зуются водой в присутствии катализатора - минеральной кислоты. Ацетали значительно более устойчивы к щелочам, чем к кислотам, и они настолько устойчивее свободных альдегидов по отношению к действию оснований и окислителей, что соединения, содержащие альдегидную группу, часто превращают в ацетали для защиты этой группы во время синтетических операций с участием других групп молекулы. Ацетали обычно получают путем пропускания около 1 % газообразного хлористого водорода в раствор альдегида в метаноле или этаноле. [14]
Ацетали и кетали имеют у одного углеродного атома две эфирные группы и являются гораздо более реакционноспособными соединениями, чем простые эфиры. В присутствии кислых катализаторов они быстро гидро-лизуются в соответствующие карбонильные соединения. Альдегиды могут быть защищены превращением их в ацетали, которые в отличие от альдегидов устойчивы в щелочной среде. [15]
Страницы: 1 2 3 4