Ацеталь-дегид
Cтраница 1
Образующийся ацеталь-дегид сорбируется из реакционной смеси водой. [1]
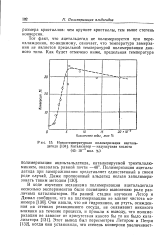 |
Низкотемпературная полимеризация ацеталь-дегида. Катализатор - надуксусная кислота ( 45. КГ3 мол. %. [2] |
Полимеризация ацеталь-дегида при замораживании представляет единственный в своем роде случай. [3]
С водой ацеталь-дегид дает гидрат состава CFLCHOH О ( апьдегид-рат СН СН ( ОН)), который, однако, не стоек и не может быть выделен из раствора. [4]
Аналогично гидрирование ацеталь-дегида сопровождается передачей двух электронов от молекулы водорода. [5]
Ингибирует окисление ацеталь-дегида in vivo, вероятно, путем инги-бирования глицеральдегиддегидроге-назы. [6]
В присутствии ацеталь-дегида образуется ярко-зеленое кольцо. [7]
Термическое разложение газообразного ацеталь-дегида является бимолекулярной реакцией. [8]
При окислении пропана получают ацеталь-дегид, формальдегид, уксусную кислоту, ацетон. [9]
Обнаружены также этилацетат и ацеталь-дегид. На рис. 25 и 26 показано влияние на окисление количеств резината марганца и температуры. [10]
При конденсации ж-толуилендиамина и ацеталь-дегида образуется краситель основной желтый Н ( эухризин GGNX), а при конденсации и-толуилен-диамина с бсизальдепгдом - краситель бензофлавин. [11]
Сырьем для промышленного производства ацеталь-дегида служат этанол, ацетилен и этилен. [12]
Однако парофазный метод получения ацеталь-дегида из ацетилена может иметь значение при использовании смесей ацетилена с водяным паром или другими и н ертными газами. [13]
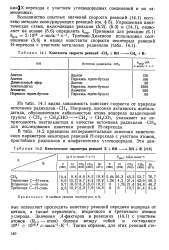 |
Константы скорости реакций СН3 RH.| Кинетические параметры реакций X - f RH. [14] |
Например, высокая активность ацеталь-дегида, обусловленная лабильностью атома водорода альдегидной группы ( - СН3 СН3СНО - - - - СН4 СН3СО), указывает на непригодность ацетальдегида в качестве источника радикалов - СН3 для исследования кинетики реакций Н - перехода. [15]
Страницы: 1 2 3 4