Ацетилглюкозамин
Cтраница 2
ЛИЗОЦЙМ ( мурамидаза), фермент класса гидролаз, катализирующий гидролиз ( 3 - 1 - 4-гликозидной связи между остатками М - ацетилглюкозамина и М - ацетил-мураминовой к-ты ( см. ф-лу) пептидогликана клеточной стенки бактерий. Гидролизует также такую же связь в полимере, состоящем из остатков М - ацетилглюкозамина ( хитине), но со значительно меньшей скоростью. [16]
При гидролизе в жестких условиях она распадается на глюкуроно-вую кислоту и глюкозамин, в более мягких условиях выделяется дисахарид - глюкуронадо-1, 4 - М - ацетилглюкозамин. [17]
Условные обозначения остатков моносахаридов и аминокислот глюкозы - С1с, глюкуроновой к-ты О1сА, галактозы - Оа1, ксилозы - Ху14 М - аце-тилгалактозамина - СЫНАс, Н - ацетилглюкозамина СНсКАс, сиаловой к-ты ЗА, маннозы Мап, серина 8ег, треонина Тпг, аспарагшш Азп. [18]
При образовании полисахаридов в клетках млекопитающих из фруктозы образуется фруктозо-6 - фосфат, затем глюкозамин-6 - фосфат и в конечном итоге - М - ацеТилман - нозамин, UOP-N - ацетилглюкозамин, UOP-N - ацетилгалак-тозамин. [19]
ХИТИН, полисахарид, образованный остатками аминосахара ацетилглюкозамина. У грибов заменяет целлюлозу, с к-рой сходен по хим. и физ. Длинная льняная или шерстяная рубаха, чаще без рукавов. Паразитируют на пресноводных и мор. [20]
ХИТИН, полисахарид, образованный остатками аминосахара ацетилглюкозамина. У грибов заменяет целлюлозу, с к-рой сходен по хим. и физ. Длинная льняная или шерстяная рубаха, чаще без рукавов. [21]
В некоторых видах соединительной ткани ( например, в роговице глаза) наряду с иукополиуронидами был обнаружен особый мукополисахарид, получивший название кератосульфата, или кератосерной кислоты. В состав кератосульфата входят в эквивалентном количестве галактоза, ацетилглюкозамин и серная кислота. [22]
ЛИЗОЦЙМ ( мурамидаза), фермент класса гидролаз, катализирующий гидролиз ( 3 - 1 - 4-гликозидной связи между остатками М - ацетилглюкозамина и М - ацетил-мураминовой к-ты ( см. ф-лу) пептидогликана клеточной стенки бактерий. Гидролизует также такую же связь в полимере, состоящем из остатков М - ацетилглюкозамина ( хитине), но со значительно меньшей скоростью. [23]
Углеводная часть ФСГ составляет ок. В ее состав входят В-ман-ноза, В-галактоза, Ь - фукоза, 1Ч - ацетилглюкозамин, 1Ч - ацетил-галактояамин и сиаловаа к-та. Каждая из субъединиц ФСГ содержит по 2 олигосахаридные цепи, соединенные с полипептидной цепью 14-гликозидной связью, образуемой остатками К-ацетилглюкозамина и амидной фуппой остатков аспарагина. [24]
Химическое отверждение и микрокристаллизация часто встречаются в биологических аналогах жидких кристаллов и, в частности, во внешних покровах насекомых. Их материал состоит из белков, отвержденных фенольным дублением, и хитина - микрокристаллического линейного полимера ацетилглюкозамина. Однако цепи хитина образуют нематические и холестерические псевдоморфозы. В этом примере два главных соединения, создавая сложный материал, взаимодействуют двумя различными способами. При образовании панцирей ракообразных, органическая матрица которых является холестерической псевдоморфозой, откладывающийся первым материал выделяется в состоянии двоякопреломляющего геля. Последний быстро микрокристаллизуется с образованием гликопротеиновых связей. Фенольное дубление в этом случае обычно действует слабо. [26]
Он действует на пептидогликано-вый остов микробной стенки, где специфически гидролизует 1 4 гликозид-ные связи между N-ацетилмурамовой кислотой и М - ацетилглюкозамином. В небольших концентрациях лизоцим постоянно присутствует в сыворотке крови, мокроте, слезах и других биологических жидкостях. [27]
Многие из указанных выше эффектов можно прекрасно проиллюстрировать на примере механизмов связывания и катализа, осуществляемых ферментом лизоцимом. NAG), связанных 3 - 1 - 4-гликозидными связями, однако большая часть работ по изучению механизма была проведена на более простых субстратах. Так, поли - Л - ацетилглюкозамин также гидролизуется ферментом, однако эффективность этой реакции существенно зависит от размера субстрата и трисахарид ( NAG) 3 фактически является ингибитором лизоцима. Сравнение трехмерных структур фермента и комплекса последнего с ( NAG) 3 показывает, что трисахарид связывается во впадине фермента. Такое сравнение позволяет детально исследовать связывание трех моно-сахаридных звеньев ( NAG) 3 в участках А, В и С фермента, которое осуществляется посредством комбинации гидрофобных в - чимодействий и водородных связей. [28]
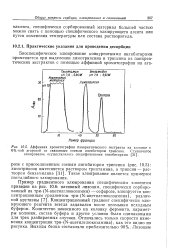 |
Аффинная хроматография панкреатического экстракта на колонке с. [29] |
Отличались только скорости изменения концентрации три - ( М - ацетилглюкозамина), как это видно из рисунка. [30]
Страницы: 1 2 3
