Литий
Cтраница 1
Литий, его химия и технология, Госатомиздат, 1960, стр. [1]
Литий и натрий таких соединений не образуют, что является отражением общей закономерности увеличения прочности комплексных гексагалогенотитанатов ( цирконатов и гафнатов) с увеличением радиуса иона щелочного металла. [2]
Литий вследствие малого радиуса атома имеет относительно прочную кристаллическую решетку, что подтверждается сравнительно высокой температурой плавления. [3]
Литий и натрий получают электролизом их расплавленных хлоридов. [4]
Литий вводят в состав некоторых сплавов. Натрий применяют при синтезах различных органических соединений. Он является исходным веществом для получения перекиси натрия Na2O2, a также входит в состав сплавов, идущих для производства подшипников. [5]
Литий хотя и типичный щелочной элемент, тем не менее занимает среди них особое положение: по свойствам он как бы переходный к элементам главной подгруппы II группы периодической системы. Так, следует отметить малую растворимость карбоната, фосфата и фторида лития, характерную также для однотипных солей щелочноземельных элементов. Кроме того, литий образует типы соединений, отсутствующие у других щелочных элементов, а некоторые соединения ( например, нитрид лития) по условиям образования и свойствам больше напоминают соответствующие производные магния и кальция. [6]
Литий открыт в 1817 г. шведским химиком А. [7]
Литий - весьма пластичный и вязкий металл, хорошо обрабатывается прессованием и прокаткой, легко протягивается в проволоку [1], свободно режется ножом. [8]
Литий стоит первым в ряду напряжений: его нормальный потен - циал - 3 02 В [10] - наиболее отрицательный из всех известных, что объясняется сильной гидратацией ионов Li, значительно превышающей таковую ионов других щелочных металлов. Среди них ион лития имеет наибольший радиус и наименьшую подвижность, поэтому выделить литий электролизом из водных растворов солей нельзя. Это соответствует характеру изменения энергии ионизации в ряду щелочных металлов и определяет возможность получения лития электролизом из расплавов. [9]
Литий непосредственно соединяется с фтором, хлором и бромом, а при нагревании - с иодом, образуя соли. При нагревании взаимодействует с расплавленной серой и ее парами, двуокисью углерода, углеродом и кремнием. При нагревании ( 500 - 800Ч) соединяется с водородом, образуя гидрид LiH. Уже при комнатной температуре литий медленно реагирует с азотом воздуха, образуя нитрид; при 250 реакция усиливается. В токе сухого азота взаимодействие протекает быстро ( при нагревании - с воспламенением) с полным переходом лития в нитрид. [10]
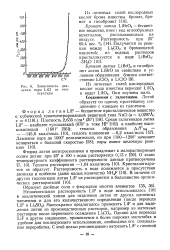 |
Зависимость давления пара LiCl от температуры. [11] |
Литий образует по одному простейшему соединению с каждым из галогенов. [12]
Литий образует несколько бинарных соединений с серой - нормальный сульфид и полисульфиды. [13]
Литий образует два бинарных соединения с азотом и несколько соединений, содержащих помимо азота другие неметаллы, из которых здесь будут рассмотрены только соединения, содержащие водород. [14]
Литий образует несколько бинарных соединений с фосфором, большинство из которых, несомненно, индивидуальные соединения. [15]
Страницы: 1 2 3 4