Достижение - предельный ток
Cтраница 3
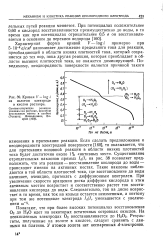 |
Кривая V - log i. [31] |
Характерная форма кривой V - log i примерно при 5 - 10 - 6а / сж2 напоминает достижение предельного тока для реакции, преобладающей в области низких плотностей тока, который сохраняется до тех пор, пока другая реакция, которая преобладает в области высоких плотностей тока, не окажется доминирующей. [32]
Однако при осаждении металла из водного раствора соли плотность тока нельзя повышать неограниченно, так как после достижения предельного тока сдвиг потенциала станет настолько велик, что потенциал катода достигнет величины, при которой возможен интенсивный разряд других имеющихся в растворе ионов, например ионов водорода. Осадок может получиться рыхлым, дендритообразным или губчатым; выход металла по току резко падает. [33]
Однако при осаждении металла из водного раствора соли плотность тока нельзя повышать неограниченно, так как после достижения предельного тока сдвиг потенциала станет настолько велик, что потенциал катода достигнет величины, при которой возможен интенсивный разряд других имеющихся в растворе ионов, например ионов водорода. Осадок может получиться рыхлым, дендритообраз-ным или губчатым; выход металла по току резко падает. [34]
В связи с высокой величиной тока обмена и малой растворимостью молекулярного водорода уже при малых поляризациях наблюдается достижение предельного тока диффузии. На рис. 24 приведены поляризационные кривые на платиновом вращающемся дисковод. При малых скоростях вращения ( т, об / мин) величина тока в широком интервале потенциалов не зависит от ф и пропорциональна т1 / г. Согласно теории дискового электрода Левича [ см. (1.104) и (1.108), § 1.5 ], это указывает на то, что земедленной стадией является диффузия молекулярного водорода в растворе. [35]
В связи с высокой величиной тока обмена и малой растворимостью молекулярного водорода уже при малых поляризациях наблюдается достижение предельного тока диффузии. На рис. 24 приведены поляризационные кривые на платиновом вращающемся дисковом электроде [50], использование которого позволяет обеспечить проведение исследований в определенных диффузионных условиях. При малых скоростях вращения ( т, об / мин) величина тока в широком интервале потенциалов не зависит от ср и пропорциональна т1 / г. Согласно теории дискового электрода Левича [ см. (1.104) и (1.108), § 1.5 ], это указывает на то, что земедленной стадией является диффузия молекулярного водорода в растворе. [36]
При определении парциальных кривых ( см. рис. 88) выявлено, что водород начинает выделяться на катоде после достижения предельного тока металла при потенциале, величина которого меньше равновесной для данного раствора. Разница между этими потенциалами является весьма заметной и превышает 0 3 в. Причина этого явления, по-видимому, заключается в уменьшении энергии активации разряда ионов водорода при образовании системы Pd - Н [6], а также в понижении рН в прикатодном слое при выделении металла. [37]
Осадки, полученные из водных и неводных растворов, представляли собой рыхлые образования, очевидно, вследствие того, что электролиз осуществлялся в условиях достижения предельного тока по сурьме. [38]
В электролитах, приготовленных на основе соли калия, хорошие осадки можно получать и без специальной чистки растворов, если в них присутствуют нитрат-ионы; ухудшения структуры осадков не происходит вплоть до достижения предельного тока диффузии разряжающихся ионов серебра. Возможно, что ионы МОз - хорошо адсорбируются поверхностью серебра и препятствуют адсорбции посторонних примесей. По этой же причине, вероятно, в электролитах, содержащих нитраты, поверхностно-активные вещества не влияют на структуру покрытий, тогда как в отсутствие NO3 - добавление ПАВ способствует образованию блеска. Таким образом, для приготовления и корректирования состава электролита лучше применять цианид калия и растворять нитрат серебра, не переводя его в хлорид, как это делалось обычно. [39]
В электролитах, приготовленных на основе соли калия, хорошие осадки можно получать и без специальной чистки растворов, если в них присутствуют нитрат-ионы; ухудшения структуры осадков не происходит вплоть до достижения предельного тока диффузии разряжающихся ионов серебра. Возможно, что ионы NO3 - хорошо адсорбируются поверхностью серебра и препятствуют адсорбции посторонних примесей. По этой же причине, вероятно, в электролитах, содержащих нитраты, поверхностно-активные вещества не влияют на структуру покрытий, тогда как в отсутствие NO3 - добавление ПАВ способствует образованию блеска. Таким образом, для приготовления и корректирования состава электролита лучше применять цианид калия и растворять нитрат серебра, не переводя его в хлорид, как это делалось обычно. [40]
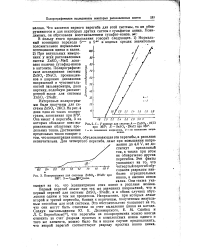 |
Подпрограмма для системы ZnSO, 2NaBr при более отрицательных.| J - V кривые для систем. А - ZnSC4 2КС1. [41] |
Она имеет 4 перегиба, 3 из которых обладают ясно выраженными областями предельных токов. Достижение предельных токов говорит о том, что концентрация ионов, обусловливающая эти перегибы, в расплаве незначительна. Для четвертого перегиба, даже при повышении напряжения до 4.0 V, не достигнут предельный ток, а также при этом не обнаружено других перегибов. [42]
В самом деле, до предельного тока концентрации ионов Н и ОН в прилегающих к мембране слоях электролита, а следовательно, и в самой мембране, малы, по сравнению с концентрацией ионов электролита, и их перенос незначителен. При достижении предельного тока концентрация электролита в обессоленных диффузионных слоях становится сравнимой с концентрацией ионов Н и ОН, образовавшихся в результате диссоциации воды, поэтому перенос этих ионов на участке предельного тока быстро нарастает. Однако при больших значениях плотности тока тенденция к увеличению переноса ионов Н и ОН вновь понижается, так как изменение рН в диффузионных слоях вызывает уменьшение концентрации ионов ОН у поверхности анионитовой мембраны и водородных ионов Н у поверхности катионитовой мембраны. [43]
 |
Схема перехода водорода. [44] |
В зоне верхней ветви кривой разряжаются молекулы воды, что требует большей энергии активации, и здесь замедленная рекомбинация заменяется на замедленный разряд. Переход от нижнего участка к верхнему наблюдается при достижении предельного тока для гидроксониевых ионов. [45]
Страницы: 1 2 3 4 5