Лыгин
Cтраница 2
Из спектроскопических данных Киселев и Лыгин ( 1961а) рассчитали колебательную, вращательную и конфигурационную энтропии воды, адсорбированной на гидроксилированной поверхности кремнезема. Для адсорбированной воды были выбраны две модели, в первой из них вода связана водородной связью с одной, - а во второй - с двумя гидроксильными группами. Рассчитанные значения энтропии были меньше, чем экспериментально определенные, что указывает на наличие других степеней свободы подвижности молекул, возможно колебаний параллельно поверхности, дающих вклад в экспериментальные значения энтропии. Аналогичные расчеты были предприняты ( Киселев, Лы-тин, 19616) для случая взаимодействия между поверхностными гидроксильными группами и физически адсорбированным бензолом и к-гексаном. [16]
Из спектроскопических данных Киселев и Лыгин ( 1961 а) рассчитали колебательную, вращательную и конфигурационную энтропии воды, адсорбированной на гидроксилированной поверхности кремнезема. Для адсорбированной воды были выбраны две модели, в первой из них вода связана водородной связью с одной, - а во второй - с двумя гидроксильными группами. Рассчитанные значения энтропии были меньше, чем экспериментально определенные, что указывает на наличие других степеней свободы подвижности молекул, возможно колебаний параллельно поверхности, дающих вклад в экспериментальные значения энтропии. Аналогичные расчеты были предприняты ( Киселев, Лыгин, 19616) для случая взаимодействия между поверхностными гидроксильными группами и физически адсорбированным бензолом и w - гексаном. [17]
Как уже было отмечено, Киселев и Лыгин считают, что образование связанных гидроксильных групп обусловлено неупорядоченным расположением кремниевых тетраэдров на поверхности. Возможно, что высокое относительное содержание свободных гидроксильных групп на кремнеземах, полученных гидролизом в пламени четыреххлористого кремния, обусловлено использованием высоких температур в процессе их приготовления. Частицы таких кремнеземов хорошо прокаливаются, в результате чего неупорядоченность в расположении кремниевых тетраэдров на поверхности может быть уменьшена, так что гидроксильные группы не сближаются на расстояние, необходимое для образования водородной связи. [18]
С целью выяснения процесса формирования структуры скелета ксерогелей Киселев, Лыгин, Неймарк, Слинякова и Чэнь Вэнь-хан [58] провели электронно-микроскопическое исследование золей кремневой кислоты и полученных из них гидрогелей и ксерогелей. Ксерогели были изучены также адсорбционным методом. [19]
С целью изучения участия поверхностных гидроксильных групп кремнеземов в адсорбционном взаимодействии в условиях обычных адсорбционных измерений Галкин, Киселев и Лыгин [39, 41] исследовали изменение интенсивности полосы поглощения валентных колебаний гидроксильных групп при адсорбции воды, в условиях, исключающих нагревание образца инфракрасной радиацией. Как следует из приведенных на рис. 50 спектрограмм [39], адсорбция молекул воды на аэросиле в условиях, исключающих нагрев образца инфракрасно радиацией, сопровождается резким уменьшением интенсивности полосы свободных гидроксильных групп поверхности кремнезема вплоть до полного ее исчезновения из спектра. [20]
 |
Спектр поверхностных гидрокспльных групп порошка кабосила. McDonald ( 1957, J. Am. chem. Soc., 79, 850. [21] |
Неожиданно возникшим затруднением в подобных исследованиях, как отмечали в обзорных статьях Эйшенс и Плискин ( 1958), а также Киселев и Лыгин ( 1962), было исчезновение обертонной полосы поглощения гидроксильных групп после адсорбции полярных молекул. [22]
При адсорбции молекул, имеющих атомы со свободными электронными парами и способных, кроме того, к образованию взаимной водородной связи, а именно молекул CD3OD ( Геодакян, Киселев, Лыгин, 1967а) и NH3 ( Геодакян, Киселев, Лыгин, 1968), дегЧствие катионов при малых степенях заполнения поверхности полостей проявляется как препятствие к образованию прочной водородной связи между молекулами. При этих степенях заполнения положение полос поглощения валентных колебаний NH ц ОН этих молекул чувствительно к типу обменного катиона. [23]
При адсорбции молекул, имеющих атомы со свободными электронными парами и способных, кроме того, к образованию взаимной водородной связи, а именно молекул CD3OD ( Геодакян, Киселев, Лыгин, 1967а) и NH3 ( Геодакян, Киселев, Лыгин, 1968), дегЧствие катионов при малых степенях заполнения поверхности полостей проявляется как препятствие к образованию прочной водородной связи между молекулами. При этих степенях заполнения положение полос поглощения валентных колебаний NH ц ОН этих молекул чувствительно к типу обменного катиона. [24]
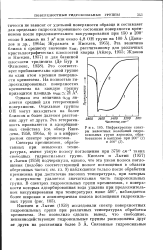 |
Инфракрасные спектры валентных колебаний гидроксильных групп аэросила, обработанного в вакууме при 200 ( 7 и 400 ( 2. [25] |
Спектры кремнеземов, обработанных при невысоких температурах, имеют узкую полосу поглощения при 3750 см 1 таких свободных гидроксильных групп. Киселев и Лыгин ( 1957) и Лыгин ( 1958) подчеркнули, однако, что эта узкая полоса поглощения ( подобно соответствующей полосе поглощения в области обертонных частот; см. гл. [26]
Кузьменко показала ( 1967), что адсорбированные цеолитом СаХ молекулы Н20 вследствие сильной поляризации связей ОН становятся источником протонов для образования ионов NHJ при адсорбции таким цеолитом молекул NHa. Киселев, Лыгин, Московская ( 1966) установили, что электростатическое поле цеолитов переводит практически все адсорбированные молекулы 1 2-дихлорэтана в гсн-форму. [27]
Вполне вероятно, что можно было бы избежать существующей путаницы относительно наличия адсорбированных карбониевых ионов и адсорбированных свободных радикалов, если бы были проведены одновременные исследования методами инфракрасной спектроскопии и электронного парамагнитного резонанса. Киселев и Лыгин ( 1962) подчеркивали преимущества совместного использования инфракрасной спектроскопии с классическими адсорбционными и калориметрическими исследованиями. [28]
Когда на кремнеземе адсорбируется грег-бутиловый спирт, то легко обнаруживается формирование водородных связей. Давыдов, Киселев и Лыгин [150] нашли, что спиртовая гидроксиль-ная группа связывается водородной связью только со свободными группами SiOH на кремнеземной поверхности, но не с си-ланольными группами, которые оказываются достаточно близко расположенными друг к другу и связываются водородными связями. Третичный спирт, кроме того, не взаимодействует с образованием связанного с поверхностью сложного эфира в той степени, как это имеет место для первичного и вторичного спиртов. Джигит, Киселев и др. [151] обнаружили, что теплота адсорбции составляла 18 ккал / моль, но она резко понижалась, если поверхность кремнезема дегидратировалась вследствие уменьшения числа образующихся водородных связей. Вероятно, метильная группа спирта имела возможность при адсорбции связываться с гидрофобным силоксановым участком поверхности, ггримыкаю-щим к силанольной группе. [29]
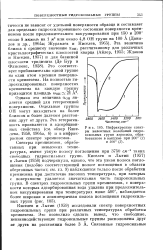 |
Инфракрасные спектры валентных колебаний гидроксильных групп аэросила, обработанного в вакууме при 200 ( 7 и 400 ( 2. [30] |
Страницы: 1 2 3