Аэросила
Cтраница 2
Адсорбция неассоциированных анионов ПАВ на аэросиле, как мы видели в главе II, приводит к относительно прочному закреплению концевых метильных групп углеводородных радикалов ПАВ и очень слабому взаимодействию анионогенных полярных групп с поверхностью, вследствие чего адсорбированные ионы под влиянием теплового движения осциллируют во всех возможных направлениях вокруг закрепленного конца неполярного радикала. [17]
Адсорбция пара уксусной кислоты на аэросиле не приводит к появлению интенсивных полос поглощения в области 1400 - 1600 смГ1, следовательно, в этом случае ее ионы не образуются. Узкая полоса поглощения свободных поверхностных гидроксилов аэросила при 3750 см 1 исчезает из спектра, а вместо нее появляется широкая полоса в области 2500 - 4300 смГ1, характерная для поглощения связанных поверхностных гидроксилов и гидроксилов карбоновой кислоты. Таким образом, молекулы уксусной кислоты взаимодействуют с поверхностными гидроксилами кремнезема только молекулярно. [18]
Адсорбция пара уксусной кислоты на аэросиле не приводит к появлению интенсивных полос поглощения в области 1400 - 1600 смГ1, следовательно, в этом случае ее ионы не образуются. Узкая полоса поглощения свободных поверхностных гидроксилов аэросила при 3750 см-1 исчезает из спектра, а вместо нее появляется широкая полоса в области 2500 - 4300 смГ1, характерная для поглощения связанных поверхностных гидроксилов и гидроксилов карбоновой кислоты. Таким образом, молекулы уксусной кислоты взаимодействуют с поверхностными гидроксилами кремнезема только молекулярно. [19]
Анализ энтропии адсорбции ММА на аэросиле ( рис. 2.12) показал, что с изменением степени заполнения поверхности механизм адсорбции изменяется. [21]
Величина статической ДП адсорбированной на аэросиле воды в пределах заполнения до 2 5 БЭТ-монослоев остается приблизительно постоянной, в то время как при адсорбции воды на пористом силикагеле она существенно уменьшается начиная с субмонослой-ных покрытий, что, вероятно, связано со структурированием воды в порах силикагеля. [22]
 |
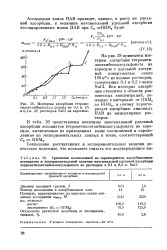
Изотермы адсорбции паров хлороформа ( /, бензола ( 2, диоксана ( 3 и метанола ( 4 на аэросиле. [23] |
Итак, по величине сродства растворителей к аэросилу можно записать ряд: вода, диметилформамид метанол диоксан бензол хлороформ. Теперь, зная термодинамическое качество растворителей и сродство их к адсорбенту, данные по адсорбции можно объяснить следующим образом. Сополимеры окиси этилена незначительно сорбируются на аэросиле из растворов в ДМФ из-за сильного сродства растворителя к адсорбенту. Величина адсорбции указанных полимеров из растворов в метаноле также невелика по этой же причине, но в данном случае наблюдается резкая зависимость адсорбции от молекулярного веса. Вода является умеренным по силе растворителем для сополимеров окиси этилена и, несомненно, сильно сорбируется на поверхности аэросила; тем не менее адсорбция из воды выше, чем из метанола. [24]
Оценим эту величину для диффузии ВА на аэросиле. Полученные значения AS / приближаются к величине ASa для ВА, вычисленной в предположении потерь молекулой поступательной степени свободы. Все это позволяет предположить, что преодоление потенциального барьера, связанное с частичной десорбцией молекулы, сопровождается размораживанием поступательной степени свободы, потерянной при адсорбции. [25]
Так, для рассматриваемой системы ВА-4-ВП на аэросиле рассчитанные по формулам (3.35) и (3.36) соотношения Ац / А12 и 22 / 21 оказались равными 5 - Ю 3 и 0 8 104 соответственно. Иначе говоря, слабосвязанный мономер присоединяется к макрорадикалу как со слабо -, так и с сильносвязанным концевым звеном с большей потерей энтропии, чем сильносвязанный мономер. [26]
На рис. 38 приведены изотермы адсорбции тетрамети-локтанбензолсульфоната на аэросиле с удельной доступной поверхностью около 160м2 / г из водных растворов, содержащих 0 1 и 0 2 г-экв / л NaCl. Вся изотерма адсорбции относится к области равновесных концентраций, лежащих в интервале от KKMj до ККМ2, и потому характеризует адсорбцию анионных ПАВ из мицеллярных растворов. [28]
Ниже приведены результаты определения поверхностных гйдроксильных групп в аэросиле и белой саже различных-марок методом ИК-спектроскопии. [29]
Общее содержание А12О3, ТЮ2 и РегО3 в аэросиле не превышает 0 1 вес. [30]
Страницы: 1 2 3 4 5