Двухвалентный марганец
Cтраница 4
Окисление двухвалентного марганца производят периодатом калия, персульфатом аммония, висмутатом натрия или двуокисью свинца. Лучшим окислителем является периодат калия. [46]
Гидроксид двухвалентного марганца Мп ( ОН) 2 находится в природе в виде пирохроита. В лабораторных условиях получается действием растворов едких щелочей на растворы солей двухвалентного марганца. Свежеосажденная Мп ( ОН) 2 представляет собой белый, рыхлый осадок, быстро буреющий на воздухе вследствие окисления. [47]
 |
Данные по окислению персульфатом. [48] |
При окислении двухвалентного марганца мы нашли, что один из трех кислородов гидратированной двуокиси марганца быстро обменивается с водой уже при промывании осадка. Обмен более чем одного атома не был найден даже при кипячении осадка с водой на протяжении нескольких часов. [49]
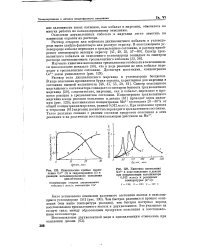 |
Кинетические кривые накопления Со3 ( 1 и гидроперекиси ( 2 в реакции катализированного окисления циклогексана.| Кинетика накопления. [50] |
Раствор соли двухвалентного марганца в углеводороде бесцветен. Спектр окисленного марганцевого катализатора совпадает со спектром бензоата трехвалентного марганца [59], следовательно, марганец, как и кобальт, переходит в процессе реакции в трехвалентное состояние. При окислении кумола и тетралина [61] марганец полностью переходит в трехвалентное состояние. [51]
Страницы: 1 2 3 4