Аминопептидаза
Cтраница 1
Аминопептидаза отщепляет в свободном виде ту аминокислоту, в которой в пептидной цепи аминогруппа будет конечной. Впрочем, обяза-1 тельно присутствие на конце цепи не столько свободной группы NH2, сколько наличие в ней, по крайней мере, одного незамещенного водорода. [1]
Аминопептидаза присутствует в слизистой оболочке кишечника, в почках, печени и селезенке, а также в дрожжах и плесени. [2]
Пептидная связь в А гидролизуется аминопептидазой, в В - карбоксипептидазой. [3]
Об использовании экзопептидаз, таких как аминопептидаза и карбоксипептидаза, для определения аминокислотной последовательности вблизи N - и С-концов белков говорилось в разд. Эндопептидазы являются протеолитическими ферментами, которые избирательно расщепляют пептидные связи в точках, удален ных от концов белковой молекулы. Эндопептидазы сильно различаются по своей специфичности. Обычно сами аминокислотные остатки с любой стороны расщепляющейся пептидной связи являются наиболее важными детерминантами специфичности про-теолитических ферментов. [4]
Как должны действовать пепсин, химотрипсин и аминопептидаза на глу-татион и окситоцин. [5]
Наконец, для определения структуры пептидов использовали акзо-пептидазы, из которых карбоксипеитидаза служит для постепенного расщепления пептидов от карбоксильного конца, а аминопептидаза - для отщепления аминокислот от аминоконца пептидов ( см. стр. [6]
К этому классу относятся протеолитические ферменты, расщепляющие пептидные связи в белках и пептидах: пепсин желудочного сока, трипсин и химотрипсин, получаемые из поджелудочной железы, аминопептидаза кишечника, папаин из сока дынного дерева и др. Специфичность действия этих ферментов зависит от их способности разрывать лишь те пептидные связи, которые находятся в определенном для каждого фермента окружении. Так, некоторые ферменты разрушают только концевые связи в белках ( экзопептидазы), другие ( эндопептида-зы) действуют на пептидные связи, лежащие далеко от концов молекулы. Кроме того, имеет значение наличие вблизи от разрываемых связей полярных групп: аминных, сульфгидрильных или оксигрупп. Протеолитические ферменты действуют только на L-формы белков и совсем не действуют на D-формы. [7]
 |
Расщепление окситоцина окситоциназой. [8] |
Недавние исследования Рыхлика [2762] позволили доказать двухстадийность инактивации окситоцина тканевыми экстрактами, протекающей через обратимое восстановление дисульфид-ной связи с образованием биологически неактивного линейного продукта и последующее необратимое расщепление дигидррок-ситоцина аминопептидазой, которая сама по себе не действует на гормон. [9]
 |
Определение С-концевой последовательности пептида с помощью кар-боксипептндаз. [10] |
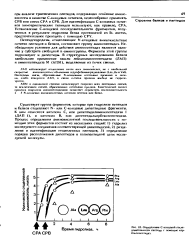
АПМ в одинаковой степени катализирует гидролиз всех пептидных связей, за исключением связей, образованных остатками пролина. Кинетический анализ процесса гидролиза аминопептидазами позволяет опредетить последовательность 2 S N-концевых аминокислотных остатков пептида или белка. [11]
Дипептидаза ( по-видимому, имеется несколько дипептидаз) расщепляет дипептиды на свободные аминокислоты. В результате ферментативного гидролиза полипептидов пептидазами ( аминопептидазой, карбок-сипептидазой и дипептидазами) в кишечнике образуются свободные аминокислоты. [12]
Протеолитические ферменты типа папаина всегда присутствуют в клетках совместно с ферментами типа пептидаз или пептид-гидролаз, которые катализируют гидролитическое расщепление пептидных связей в молекулах пептидов. Известны три группы ферментов этого типа, различающиеся по характеру их действия: аминопептидаза, карбокси пептид а-за и дипептидаза. [13]
 |
Потенциальные биомаркеры, связанные с поражением клетки. [14] |
Был проведен количественный анализ мочевых ферментов, но полноценность его была ограничена неспособностью определить происхождение фермента и отсутствием воспроизводимости результатов пробирного анализа. К исследованным ферментам относятся аминопептидаза, NAG и интестинальная щелочная фосфатаза. NAG - это, возможно, наиболее признанный маркер для контроля повреждения клеток почечных канальцев из-за его локализации в сегменте S3 канальцев. Поскольку точное клеточное происхождение и патологические причины мочевой ферментативной активности не известны, интерпретация результатов анализа вызывает затруднения. Кроме того, лекарственные препараты, диагностические процедуры и сопутствующие заболевания типа инфаркта миокарда могут затруднять интерпретацию. [15]
Страницы: 1 2 3