Политермическая диаграмма
Cтраница 1
Политермические диаграммы применяются обычно в тех случаях, когда изучаются теоретические основы политермической кристаллизации или политермического растворения. При этом необходимо рассматривать вертикальные разрезы или проекции вертикальных сечений политермы. [1]
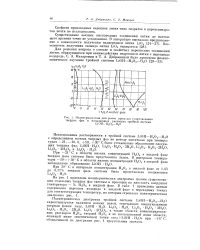 |
Цолитермичоская диаграмма пределов существования. [2] |
Политермическая диаграмма тройной системы LiOH - Н202 - Н2О характеризуется наличием восьми полей, отвечающих вышеуказанным твердым фазам: льду, LiOH Н20, Li202 Н20, Li202 Н202 ЗН20, Li202 Н202 2Н20, Li202 2Н202, а также области концентрированных растворов Н202, твердой Н202 и не исследованной нами области, лежащей ниже эвтектической точки лед-1 - LiOH Н20 при - 18 С, обозначенной на диаграмме рис. 1 треугольным значком. [3]
Политермические диаграммы растворимости двухкомпонент-ных систем ( соль - вода) изображают с помощью двух взаимно перпендикулярных координатных осей. При этом на вертикальной оси откладывают температуру, а на горизонтальной - концентрацию насыщенного раствора в процентах. Обе оси имеют конечное значение. [4]
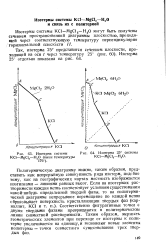 |
Изотерма системы.| Изотерма 25 системы KCI - MgCl2 - Н2О. [5] |
Политермическую диаграмму можно, таким образом, представить как непрерывную совокупность ряда изотерм, подобно тому, как на географических картах местность изображается изогипсами - линиями равных высот. Соответственно фигуративные точки с двумя твердыми фазами превращаются в политермические линии совместной растворимости. Таким образом, мерность геометрических элементов при переходе от изотермы к политерме увеличивается на единицу, и возникают новые элементы политермы - точки совместного существования трех твердых фаз. [6]
Сечение политермической диаграммы растворимости плоскостями, перпендикулярными оси температур, позволяет получить изотермические диаграммы растворимости для любой температуры. [7]
Под политермической диаграммой системы понимают изображение избранного свойства ( в данном случае растворимости) в зависимости от состава системы в некотором интервале температур. [8]
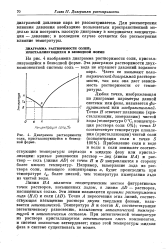 |
Диаграмма растворимости соли, кристаллизующейся в безводной форме. [9] |
Часто ее называют политермической диаграммой растворимости, так как она дает зависимость растворимости от температуры. [10]
На рис. 1 приведена политермическая диаграмма границ существования отдельных твердых фаз системы в проекции на плоскость координат температура - % Н202 в жидкой фазе. [11]
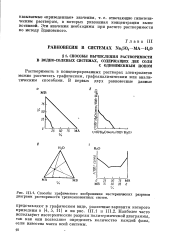 |
Способы графического изображения изотермических разрезов диаграмм растворимости трехкомпонентных систем. [12] |
Наиболее часто используют изотермические разрезы политермической диаграммы, так как они позволяют определить количество каждой фазы, если известна масса всей системы. [13]
 |
Ортогональные проекции политермы растворимости двух одноионных солей В и С в воде на координатные плоскости. [14] |
На рис. 9 приведено объемное изображение политермической диаграммы трехкомпонентной системы В-С - Н2О в прямоугольных координатах при условии кристаллизации солей в безводной форме. [15]
Страницы: 1 2 3 4