Аминоэфир
Cтраница 1
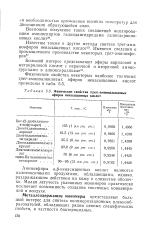 |
Физические свойства отре / п-аминоалкиловых эфиров ненасыщенных кислот. [1] |
Аминоэфиры ы р-ненасыщенных кислот являются малотоксичными продуктами, обладающими, однако, раздражающим действием на кожу и слизистые оболочки. Малая летучесть указанных мономеров практически исключает возможность создания токсичных концентраций в воздухе. [2]
Аминоэфиры нестабильны и быстро конденсируются в циклические диамиды, называемые дикетопиперазинами ( ср. Простые ангидриды или ацилхлориды получить не удается из-за легко протекающей реакции активированной карбонильной группы с аминофункцией. [3]
Аминоэфиры переведены в растворимые в воде соли: гндрохлориды, йодалкил-аты, в некоторых случаях метил-сульфометилаты с целью исследования их фармакологических свойств. [4]
Аминоэфиры более устойчивы, чем исходные карбинолами-ны, однако химическое поведение обоих классов соединений весьма схоже. Они проявляют себя как электрофильные агенты по отношению к. Например, при действии хлористого водорода или галогенангидридов карбоновых кислот 1 1-аминоэфиры превращаются в а-галогенамины R1R2NC ( R3R4) Hal ( см. разд. [5]
Аминоэфиры XXVII-XXXV обладают бронхо-спазмолитическим действием. Многие из них в дозах 0 1 - 5 мг / кг полностью снимают уже развившийся смертельный прозершювый бронхоспазм. [6]
Аминоэфиры спирогетероциклического строения [1-4] использованы в синтезе различных спирогетероциклических соединений, обладающих ценными биологическими качествами. Последний при конденсации с 1 2 - и 1 3-дигалогенидами различного строения образует тиазолидинобензо [ й ] хиназо-лины 5 и тиазинобензо [ й ] хиназолины 6, соответственно. [7]
Простые аминоэфиры типа ( 255) могут быть получены последовательностью реакций, приведенных в уравнении. [8]
Низшие алифатические простые аминоэфиры растворимы в воде. [9]
Все аминоэфиры получены известным способом-взаимодействием хлорангидридов кислот с аминоспиртами в среде нейтрального растворителя. [10]
Получение аминоэфиров протекает очень гладко, причем для проведения синтеза эквимолекулярную смесь какого-либо ароматического альдегида и малоновой кислоты нагревают в присутствии спиртового раствора аммиака в течение нескольких часов на водяной бане. По окончании нагревания спирт отгоняют, остаток растворяют в эфире, отделяют путем фильтрования от незначительного количества образующегося иногда при реакции диамида р-арилэтилен-а а-дикарбоновой кислоты RCH C ( CONH2h и затем в полученный раствор пропускают сухой хлористый водород. Хлоргидрат аминоэфира количественно выпадает из раствора в почти совершенно чистом состоянии; его отсасывают и после перекристаллизации из спирта получают химически чистый, годный для анализа продукт. В эфирном растворе остаются эфиры стиролдика рбо о-вых кислот, которые выделяют и очищают обычным методом. [11]
Из соответствующего аминоэфира таким же способом получается этилмета-крилат. [12]
Так, аминоэфиры, склонные к поликонденсации или к образованию дикетопиперазинов, могут быть получены в достаточно стабильной форме только в виде солей; это особенно важно в случае активированных эфиров аминокислот и пептидов, которые предполагается использовать для последующей циклизации. [13]
Если сравнивать аминоэфиры фуран-2 - карбоновой кислоты с амнноэфирами бромфуран-2 - карбоновой кислоты, значительной разницы в холинолитической активности в концентрации 1 10 - н не наблюдается. В концентрации 1 10 - 3 производные бромфуранкарбоновой кислоты обладают более выраженным никотииолитическим действием. [14]
Недавно ряд аминоэфиров, в том числе и эфиров а-аминокис-лот, был изучен в реакциях присоединения к инаминам33, что привело к получению интересных промежуточных соединений для синтеза пяти - и шестичленных гетероциклических систем. [15]
Страницы: 1 2 3 4