Квадратная диаграмма
Cтраница 1
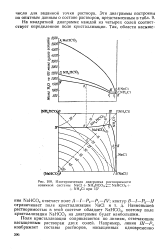
Квадратная диаграмма рассматриваемой взаимной системы ( кли-нографическая проекция пространственной диаграммы) при 15 С приведена на рис. 40, а. На этой диаграмме точки растворимости каждой из солей системы находятся в вершинах квадрата, причем соли с общим ионом ( например, NaHCO3 и NaCl или NaCl и NH4C1) расположены в смежных углах квадрата. IV, отвечающие раствору, насыщенному двумя солями, расположены на сторонах квадрата, а тройные точки Pt и Pz находятся внутри квадрата. [1]
 |
Проекция изотермы НуЮ основанию пирамиды ( вертикаль. [2] |
Квадратная диаграмма делится этими кривыми на четыре поля насыщения. [3]
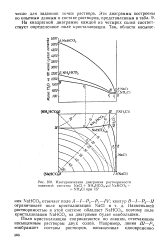
Квадратная диаграмма рассматриваемой взаимной системы ( кли-нографическая проекция пространственной диаграммы) при 15 С приведена на рис. 145, а. На этой диаграмме точки растворимости каждой из солей системы находятся в вершинах квадрата, причем соли с общим ионом ( например, NaHCO3 и NaCl или NaCl и NH4C1) расположены в смежных углах квадрата. [4]
Квадратная диаграмма указывает лишь состав солевой массы раствора. Для того чтобы определить содержание воды R растворе, необходимо прибегнуть к пространственной изотермической диаграмме четверной взаимной системы и ее водной проекции. [5]
Для квадратной диаграммы применимы правила рычага и соединительной прямой. Исходя из них, можно установить, что фигуративная точка раствора при кристаллизации ( или растворении) безводной соли движется по пути кристаллизации от вершины квадрата, лежащего в основании призматического тела. [6]
К квадратной диаграмме применимы правила рычага и соединительной прямой для графического расчета процесса кристаллизации. Однако правило рычага неприменимо для определения количества испаряемой воды, так как фигуративная точка воды удалена на водной проекции в бесконечность. Недостатком рассматриваемого типа диаграммы является относительная сложность подсчета весовых количеств испаряемой воды, выделяющейся твердой фазы и маточного раствора. [7]
 |
Изотермическая диаграмма растворимости. [8] |
На квадратной диаграмме каждой из четырех солей соответствует определенное поле кристаллизации. [9]
На квадратной диаграмме ( рис. 192) линия АО совместной кристаллизации двух солей K2SO4 и КС1 является одновременно путем кристаллизации. [10]
 |
Изотермическая диаграмма растворимости. [11] |
На квадратной диаграмме каждой из четырех солей соответствует определенное поле кристаллизации. [12]
На квадратной диаграмме ( рис. 192) линия АО совместной кристаллизации двух солей K2SO4 и КС1 является одновременно-путем кристаллизации. [13]
Из точки Ri квадратной диаграммы проводят линию кристаллизации Na2CO3 - H2O и определяют ( в ионн. Точку состава моногидрата соды откладывают на вертикальной проекции ( Ri), проводят линию кристаллизации этой соли RiM и фиксируется точка Zj пересечения линии кристаллизации с линией упаривания НРь Положение точки Z определяет количество воды на 100 молей солей в комплексе, образующемся по окончании первой стадии упаривания. [14]
 |
Схема ( примерная кубической диаграммы растворимости системы NaCl - f NH4C1 - f NH3 СО2 H2O при 15. [15] |
Страницы: 1 2 3 4 5