Трехвалентный металл
Cтраница 1
Трехвалентные металлы ( Al, Cr, Fe), образуя нитраты, дают девятиводные гидраты даже при комнатной температуре. При обезвоживании нитраты трехвалентных металлов разлагаются с отщеплением всей азотной кислоты, переходят в окислы. [1]
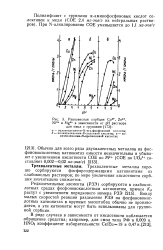 |
Равновесная сорбция Cus, Zn2. [2] |
Трехвалентные металлы хорошо сорбируются фосфорсодержащими катионитами из слабокислых растворов; по мере увеличения кислотности сорбция значительно снижается. [3]
Трехвалентные металлы хром, железо, кобальт, родий, галлий имеют близкие константы. То же наблюдается у четырехвалентных титана, церия, тория. [4]
Производные трехвалентных металлов и еют неподеленную пару электронов, поэтому многие из них исключительно бурно реагируют с акцепторами электронов. [5]
Как трехвалентный металл с координационным числом 6, алюминий валентными связями присоединяется к карбоксильным группам и координационно связывается с аминогруппами и с молекулой воды. Такие комплексы преобладают в слабокислой среде. [6]
Ацетаты трехвалентных металлов ( железа, алюминия, хрома) широко используются в качестве протравителей при окрашивании текстильных материалов. [7]
Гидроокиси трехвалентных металлов являются труднорастворимыми в воде. [8]
Хелаты трехвалентного металла с семикарбазоном салицилового альдегида ( рис. 179, Г) содержат две связанные группы ОН - ( на рис. 179 не показано) и поэтому должны быть способны к образованию полимеров с кислородным мостиком. [9]
Оксид трехвалентного металла содержит 47 1 % кислорода. [10]
Для трехвалентных металлов, образующих хелаты посредством шести координационных связей, получены более высокие значения Rf, чем для двухвалентных металлов, дающих четыре координационные связи. Ряд экспериментов по разделению произведен на силикагеле и оксиде алюминия. Масооми и Хейуорт [29] изучали 15 систем растворителей с целью разделения комплексов хрома, марганца, железа, кобальта, меди, никеля, цинка, кадмия и ртути с EDTA на микрокристаллической целлюлозе, а Вандердеелен [30] хроматогра-фировал комплексы кобальта, меди, никеля, марганца, хрома и железа с EDTA на силикагеле без связующего, причем в качестве подвижной фазы использовалось три растворителя. [11]
Карбонаты трехвалентных металлов - железа и марганца-тотчас по образовании диссоциируют на свободную углекислоту и гидраты окисей железа и марганца, к-рые, как нерастворимые в воде, остаются в рухляке. По той же схеме протекает разложение под влиянием углекислоты и алюмосиликатов, или солей алюмокремневой к-ты, с той разницей, что вместо кремневой к-ты выделяется и остается в рухляке свободная алю-мокремневая кислота ( H2Al2Si208 - H20), или каолин, в форме частиц мельче 0 001 мм. Каолин вместе с такой же крупности частицами окисей железа и марганца образует то, что называется глиной. [12]
Карбонаты трехвалентных металлов ( Al, Fe) гидролизуются нацело даже на холоду при любом разбавлении; поэтому при осаждении их вместо соли выпадает гидроокись металла. [13]
Оксид трехвалентного металла содержит 47 1 % кислорода Определите металл и напишите его электронную формулу. [14]
Окись трехвалентного металла содержит 47 1 % кислорода. [15]
Страницы: 1 2 3 4