S-аденозилметионин
Cтраница 1
Химические свойства S-аденозилметионина представляют значительный интерес. Они идентичны для всех четырех возможных диастереомеров. Как было упомянуто выше, гидролиз при значениях рН от 4 до 7 приводит к гомосерину и метилтиоаденозину. Последний при действии кислоты в более жестких условиях разлагается дальше с образованием аденина и метилтиорибозы. В результате щелочного гидролиза в мягких условиях при 0 происходит разрыв гликозидной связи в нуклеозиде и получаются аденин и S-рибо-зилметионин; при действии горячей щелочи S-рибозилметионин разлагается далее до метионина. [1]
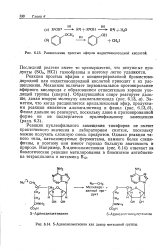 |
Расщепление простых эфиров иодистоводородной кислотой. [2] |
Аденозилгомоцистенины - 6.14. S-Аденозилметионин как донор метальной группы. [3]
После того как S-аденозилметионин теряет свою группу и образующийся S-аденозилгомоцистеин молекулой воды, образуется аминокислота гомоцистеин. В организме млекопитающих гомоцистеин может превращаться в ци-стеин, и поэтому последний не является незаменимой аминокислотой; гомоцистеин может быть превращен также в метионин при метилировании соединением, которое служит источником углеродных фрагментов ( метил, формил и др.) в биологических системах - тетрагидрофолиевой кислотой. В некоторых риях гомоцистеин может превращаться в метионин при ровании метилкобаламином ( метальным производным витамина Bj2) в присутствии других необходимых соединений или ров. Последняя из описанных реакций метилирования ляет интерес, поскольку может протекать с низкой скоростью в отсутствие ферментов, и па ее основе была создана простая модельная система ( гл. [4]
Источником метальных групп является S-аденозилметионин, ферменты - метилтрансферазы. Метиль-ной конъюгации подвергаются фенолы, амины, тиоловые соединения. Образуются соответственно О -, N - и S-метиловые конъюгаты. Процесс наиболее интенсивен в печени. [5]
Предполагают, что некоторыедекарбоксилазыживотныхтканей декарбоксилирующие, например, S-аденозилметионин, фосфатидилсерин и аспартат, также содержат пируват. [6]
На основании этих данных нуклеозиду была приписана структура S-аденозилметионина [228, 229], которая была подтверждена синтезом активного метионина. Более удачным оказался метод, в котором 2 3 - О-изопропилиден - 5 - О-п-толуолсуль - фониладенозин вводили в реакцию с гомоцистеином натрия. [7]
Для исследования стереохимических закономерностей ферментативной реакции: был использован S-аденозилметионин, в - котором содержится обладающая хиральными свойствами ме-тильная группа. [8]
В реакциях О-метшшрования в качестве донора метальных групп используется S-аденозилметионин, причем ферменты, катализирующие эти реакции, чрезвычайно специфичны как по отношению к месту метилирования, так и по отношению к классу метилируемого соединения. В нормальных условиях метилтрансферазы флавоноидов катализируют метилирование только на уровне флавонов и флавонолов и не катализируют метилирование антоцианидинов. [9]
Имеющиеся данные показывают, что донором метильной группы во всех случаях служит S-аденозилметионин. Однако и сам гли-цинбетаин может быть донором метильной группы. В табаке, например, метальные группы бетаина включаются в никотин, а в ячмене бетаин переносит метальные группы на тирании с образованием горденина. Следует отметить, что бетаины представляют собой ониевые соединения и во всех известных реакциях трансметилирования участвует метильная группа ( или группы), непосредственно связанная с центральным атомом. Реакции трансметилирования, идущие с участием бетаина, выявлены в бесклеточных препаратах из животных тканей, но не из растительных. Образование горденина и тригонеллина из S-аденозилметионина путем метилирования обнаружено в растительных экстрактах. [10]
Кентони очистил фермент, катализирующий активирование метионина, и показал, что S-аденозилметионин может служить донатором метальной группы в отсутствие аденозинтрифосфата. [11]
Препараты хроматофоров Rhodopseudomonas-spheroides катализируют этерификацию остатка пропионовой кислоты в положении 6 Mg-протопорфирина IX [133] метильной группой S-аденозилметионина. Протопорфирин IX также этерифицируется этой системой, но только в 15 раз медленнее магниевого комплекса. Это дает основание предполагать, что Mg-прото-порфирин IX является нормальным субстратом для этерификации. [12]
Выберите из предложенных вариантов процессы обмена, которые будут нарушены при недостатке фолиевой кислоты: а) образование S-аденозилметионина; б) синтез метионина из гомо-цистеина; в) синтез пуриновых нуклеотидов; г) превращение серина в глицин; д) синтез пиримидиновых нуклеотидов. [13]
 |
Биосинтез катехоламинов. [14] |
Последний из трех катехоламинов образуется в результате метилирования норадреналина с помощью фермента фенилэтаноламин - М - метилтрансферазы, использующего S-аденозилметионин в качестве донора метальных групп. Будучи темп-задающим ферментом, эта гид-роксилаза регулируется разнообразными механизмами. [15]
Страницы: 1 2 3 4