Метод - микроволновая спектроскопия
Cтраница 2
Приведенные числа наглядно показывают возможности использованного для их установления метода микроволновой спектроскопии ( III § 6 доп. Энергия связи S O оценивается в 119 ккал. [16]
Приведенные числа наглядно показывают возможности использованного для их установления метода микроволновой спектроскопии ( III § 6 доп. [17]
Приведенные числа наглядно показывают возможности использованного для их установления метода микроволновой спектроскопии ( III § 6 доп. Ионизационный потенциал молекулы SO2 равен 12 7 в, а для ее сродства к электрону Дается значение 64 ккал / моль. [18]
 |
Температурная зависимость частот ЯКР 35С1 для а - и - модификаций Са ОаСЦ. [19] |
Напомним, что константа квад-рупольного взаимодействия может быть получена методом микроволновой спектроскопии, а в гл. V увидим, что она измеряется и в мессбауэров-ской спектроскопии. [20]
Большинство из экспериментально определенных барьеров, включая барьеры, полученные методом микроволновой спектроскопии [84], было рассчитано на основании косинусоидальной зависимости и в таком виде применялось для расчетов энергий конформаций. [21]
Длины связей и углы между ними определены Флайгаром и Хо-ве [434] методом микроволновой спектроскопии, а также Хоффманом [610] методом дифракции электронов; полученные в обоих работах данные хорошо согласуются между собой. Эти данные использованы для расчета термодинамических функций. Броерс, Кетелаар и Ван Фелден [172] экспериментально установили Ттп 193 1 К и АНт 1 72 ккал / молъ. Кетелаар, Ван Фелден и Цалм [743] измеряли давление пара в температурном интервале от 240 до 372 К и установили, что ТЪ 333 8 К. [22]
Целью большинства электронографических исследований в газовой фазе, а также исследований методом микроволновой спектроскопии является прецизионное определение геометрических параметров простейших молекул для выяснения характера связи в них. [23]
Длины связей и углы между ними определены Флайгаром и Хо-ве [434] методом микроволновой спектроскопии, а также Хоффманом [610] методом дифракции электронов; полученные в обоих работах данные хорошо согласуются между собой. Эти данные использованы для расчета термодинамических функций. Броерс, Кетелаар и Ван Фелден [172] экспериментально установили Тт 193.1 К и АНт 1 72 ккал / молъ. Кетелаар, Ван Фелден и Цалм [743] измеряли давление пара в температурном интервале от 240 до 372 К и установили, что ТЪ 333 8е К. [24]
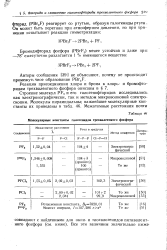 |
Молекулярные константы галогенидов трехвалентного фосфора. [25] |
Строение молекул PF3 и его галогенофторидов исследовалось как электронографически, так и методом микроволновой спектроскопии. [26]
В работе Джасиджа [ 2218а ] был впервые исследован чисто вращательный спектр JBr методом микроволновой спектроскопии. [27]
Сравнение структурных параметров молекул, найденных методом спектроскопии ориентированных молекул ( СОМ), с аналогичными параметрами, определенными методом микроволновой спектроскопии, можно найти в [20, 31, 25, 17, 16], Успешными оказались также первые попытки применения метода СОМ к определению геометрии комплексных соединений [30], Разумеется, эти соединения должны хорошо растворяться в жидком кристалле и не иметь с ним сильных межмолекулярных взаимодействий. [28]
Такое же температурное исследование 1 2 4-триазола показало присутствие при - 34 С 1Я - таутомера, тот же таутомер обнаружен в паровой фазе методом микроволновой спектроскопии. [29]
Такое же температурное исследование 1 2 4-триазола показало присутствие при - 34 С 1Я - таутомсра, тот же таутомер обнаружен в паровой фазе методом микроволновой спектроскопии. [30]
Страницы: 1 2 3 4