Метод - микроволновая спектроскопия
Cтраница 3
 |
Структура карборанов napa - CH ( BH CH. [31] |
Наибольшее применение имеют методы микроволновой вращательной спектроскопии и газовой электронографии. Методом микроволновой спектроскопии возможно исследование лишь полярных молекул ( ц07 0) при достаточном для решения структурной задачи числе изотопозамещенных производных. В методе газовой электронографии трудности определения структуры молекулы возникают в том случае, если в молекуле различные независимые расстояния близки между собой или если вклад в рассеяние каких-либо пар атомов слишком мал. [32]
В Советском Союзе первые работы по микроволновой спектроскопии были начаты в физическом институте им. Позднее метод микроволновой спектроскопии стали применять для изучения строения молекул в институте физики АН Азербайджанской ССР. [33]
Большая часть работ посвящена установлению строения простейшего представителя нитросоединений - нитрометана. Недавно методом микроволновой спектроскопии уточнены значения структурных параметров нитрометана. [34]
Грин и Холден [540] рассчитали термодинамические свойства на основании вполне допустимых отнесений колебаний, принятых длин связи и углов, метильного и скелетного барьеров внутреннего вращения, равных соответственно 3100 и 2900 кал / моль, и разности энергии между транс - и гош - вращательными изомерами, равной 50 кал / моль. Данные, полученные Сарахманом [1276] методом микроволновой спектроскопии, а также данные Морино и Кухитцу [1026], полученные методом дифракции электронов, подтверждают приведенные выше оценки; на этом основании приняты значения Грина и Холдена. [35]
Грин и Холден [540] рассчитали термодинамические свойства на основании вполне допустимых отнесений колебаний, принятых длин связи и углов, метального и скелетного барьеров внутреннего вращения, равных соответственно 3100 и 2900 кал / моль, и разности энергии между транс - и гош-вращательными изомерами, равной 50 кал / молъ. Данные, полученные Сарахманом [1276] методом микроволновой спектроскопии, а также данные Морино и Кухитцу [1026], полученные методом дифракции электронов, подтверждают приведенные выше оценки; на этом основании приняты значения Грина и Холдена. [36]
Чисто вращательные спектры газов, молекулы которых имеют постоянный дипольный момент, находятся, как известно, либо в микроволновой, либо в дальней инфракрасной области. Обычно такие спектры исследуют с помощью методов микроволновой спектроскопии, точность и разрешающая способность которых значительно превосходят возможности методов длинноволновой инфракрасной спектроскопии. Микроволновая спектроскопия используется для изучения таких явлений, как сверхтонкое расщепление и эффекты Штарка и Зеемана. С помощью таких исследований затем могут быть получены очень точные значения геометрических параметров. Техника измерений здесь в принципе проще, чем в оптическом диапазоне, поскольку вместо источника непрерывного спектра в микроволновой спектроскопии применяются высокомонохроматические клистроны с переменной частотой. Таким образом, отпадает необходимость в дифракционной решетке и удается избежать трудностей, связанных с применением системы монохроматоров; ми кроволновые методы по существу следует отнести к электронным, а не к оптическим. [37]
Результаты более ранних низкотемпературных исследований Сталла [1431] по определению теплоемкости, а также результаты Монтгомери и Де Вриса [1021] по определению теплоемкости пара хорошо согласуется с приведенными выше данными. Скотт и др. использовали результаты исследований строения методом микроволновой спектроскопии Мак-Каллоха и Полноу [945] и немного исправленные отнесения колебаний по Смиту, Фергюсону, Хадсону и Нил-сену [1377] для расчета термодинамических функций и при этом получили значения, хорошо согласующиеся с экспериментальными данными. [38]
Для некоторых молекул типа асимметричного волчка ( табл. 17) данные по DJ, полученные из микроволновых спектров и спектров КР, прекрасно согласуются. Определяя постоянные центробежного искажения для молекул типа асимметричного волчка методом микроволновой спектроскопии, Серенсен [178] пришел к выводу, что спектроскопия КР позволяет получать вполне надежные значения Дг. Однако Петзуч [266] вычислил DJ, DJK и DK для циклопентена из результатов анализа нормальных колебаний. Рассчитанное значение Дг ( 7 9 - 10 - 8 см-1) оказалось больше имеющегося экспериментального значения ( 3 75 1 25) - Ю 8 см-1 [89], а сравнение со значением ( 30 50) - 10 - 8 см-1 [179] показало, что последняя величина является нереальной. [39]
Направление диполя в молекуле фурана ( 0 72 Д) в противоположность распространенным ошибочным взглядам таково, что отрицательный заряд сосредоточен на атоме кислорода, который, таким образом, индуктивно оттягивает электроны кольца. Валентные углы и длины связей для тиофена, пиррола и фурана были определены методом микроволновой спектроскопии. В качестве критерия ароматичности было использовано соотношение длин 2 3 - и 3 4-связей, но обоснованность этого подхода подвергалась сомнению. [40]
Справочник содержит полную и систематическую сводку данных по электрическим дипольным моментам неорганических, органических, элементорганических и координационных соединений. Изложены принципы и методика определения дипольных моментов в парах, растворах и с помощью метода микроволновой спектроскопии. [41]
Колесов, Мартынов и Скуратов [793] измеряли энтальпию сгорания в атмосфере кислорода и определили hHf g) - 178 2 ккал / моль, Рассел, Голдинг и Иост [1270] опубликовали следующие низкотемпературные данные: Tip 161 82 К, ДЯттг 1 480 ккал / молъ, ТЪ 225 86 К и Mfv 4 583 ккал / молъ при 224 40 К. Эджел, Миллер и Эми [367], а также Томас, Хикс и Шеридан [1484] проводили исследования методом микроволновой спектроскопии и получил практически идентичные общие моменты инерции, хотя интерпретация этих авторов различается. Ыилсен, Клаасен и Смит [1070] опубликовали общепринятые отнесения колебаний. На основании этих данных, а также величины энтропии, определенной по третьему закону термодинамики, был установлен барьер внутреннего вращения 3200 кал / моль. [42]
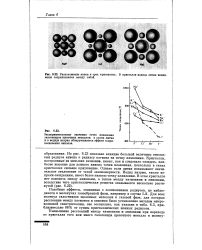 |
Расположение ионов в трех кристаллах. В кристалле иодида лития иодид-ионы соприкасаются между собой. [43] |
Подобные эффекты, связанные с соотношением радиусов, не наблюдаются в молекулах газообразной фазы, например в случае Lil. Для всех молекул галогенидов щелочных металлов в газовой фазе, для которых расстояние между катионом и анионом было установлено методом микроволновой спектроскопии, оно составляет, как указано в табл. 6.3, приблизительно 86 % от суммы кристаллических ионных радиусов. [44]
Бартелл и Бро-куей [79] определили длины связей и углы, воспользовавшись методом дифракции электронов, и получили данные, хорошо согласующиеся со значениями, установленными методом микроволновой спектроскопии. [45]
Страницы: 1 2 3 4