Диазиридин
Cтраница 2
Реакция N-незамещенных амидинов с галогенирующими агентами, например с гипобромитом или гипохлоритом натрия [347], приводит к диазиридинам. Иногда удается выделить N-моногалоген-интермедиаты этих реакций. [16]
Диазиридины могут быть получены из кетонов реакцией с аммиаком или первичными аминами в присутствии аминирующих агентов, таких, как хлороамин или гидроксиламин - О-сульфо кислота. Диазиридины также синтезируют электроциклизацией стабилизированных азометинимидов при облучении УФ-све-том. [17]
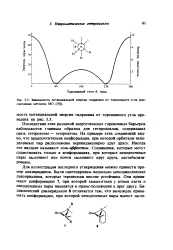 |
Зависимость потенциальной энергии гидразина от торсионного угла ( рассчитанная методом МО. [18] |
Были синтезировны несколько моноциклических диазиридинов, которые термически вполне устойчивы. Они принимают конформацию 7, при которой заместители у атома азота и неподеленные пары находятся в транс-положении к друг другу. [19]
Максимально ограничена конформационная свобода в диазиридинах: здесь приходится делать выбор лишь между цил - и гра с-расположение. ФЭС позволяют однозначно определить конформацию. По причинам как стерическим, так и взаимодействия неподеленных пар, преобладать должна г / го - конформация. Не эмпирические расчеты [76] дают для самого диазиридина преимущественно T / ww - формы в 34 кДж / моль. Угол 102, определенный для 1, 2-диметилдиазиридина в работе [ 491, совпадает с определенным для тетраалкилгидразинов ( табл. 2), что указывает на оптимальное расположение неподеленных пар в транс-форме. [20]
Эта реакция формального циклоприсоединения имеет широкие области применения, при использовании самого хлорамина ( или подобного ему реагента, гидроксиламин - О-сульфокислоты) или N-замещенных хлораминов в реакцию вступают разнообразные шиффовы основания - производные альдегидов и ациклических и циклических кетонов. Во многих случаях шиффово основание можно превратить в диазиридин in situ с выходом 50 - 80 %, проводя реакцию карбонильного соединения с аммиаком или первичным или вторичным амином в присутствии гидроксиламин - О-сульфокислоты или N-замещенной гидроксиламин - О-сульфокислоты. По-видимому, диазиридин образуется в результате первоначального нуклеофильного присоединения по двойной связи углерод-азот и последующего замыкания цикла с одновременным отщеплением. [21]
Устойчивую конфигурацию имеет азот и в других трехчленных циклах, например в диазиридинах. Соединение ( 59) получил в оптически активном виде Р. Г. Костяновский [29]; барьер рацемизации равен 85 - 100 кДж / моль. Оптически активные диазиридины ( 60) - ( 62) хро-матографированием рацематов на триацетилцеллюлозе получил также А. Маншрек [30]; барьеры рацемизации для них составляют 110 кДж / моль. [22]
Эта реакция формального циклоприсоединения имеет широкие области применения, при использовании самого хлорамина ( или подобного ему реагента, гидроксиламин - О-сульфокислоты) или N-замещенных хлораминов в реакцию вступают разнообразные шиффовы основания - производные альдегидов и ациклических и циклических кетонов. Во многих случаях шиффово основание можно превратить в диазиридин in situ с выходом 50 - 80 %, проводя реакцию карбонильного соединения с аммиаком или первичным или вторичным амином в присутствии гидроксиламин - О-сульфокислоты или N-замещенной гидроксиламин - О-сульфокислоты. По-видимому, диазиридин образуется в результате первоначального нуклеофильного присоединения по двойной связи углерод-азот и последующего замыкания цикла с одновременным отщеплением. [23]
Несмотря на сильно напряженную структуру, ЗЯ-диазирины удивительно нереакционноспособны. Они не изменяются при действии щелочей и в отличие от диазоалканов не взаимодействуют с кислотами или другими электрофильными реагентами. Они вступают, однако, в реакцию с гриньяровскими реагентами при О С, давая 1-замещенные диазиридины. Сходным образом присоединяются и другие металлоорганические реагенты. [24]
Несмотря на сильно напряженную структуру, ЗЯ-дназнрины удивительно нереакционноспособны. Они не изменяются при действии щелочей и в отличие от диазоалканов не взаимодействуют с кислотами или другими элсктрофилышми реагентами. Они вступают, однако, в реакцию с гриньяровскими реагентами при О С, давая 1-замещенные диазиридины. Сходным образом присоединяются и другие металлоорганические реагенты. Напротив, при действии сильных восстанавливающих агентов диазиридины образуются только как трудно выделяемые интермедиаты, поскольку процесс сопровождается дальнейшим восстановлением с раскрытием цикла и образованием аммиака и аминов. [25]
Замещенные Диазиридины могут существовать в изомерных формах из-за медленной инверсии атома азота ( см. гл. ЗН-Диазирины 11 представляют собой циклические изомеры диазоалканов. Действительно, некоторые диазирины были получены в результате фотоизомеризации диазоалканов, но наиболее общим методом синтеза таких соединений служит окисление N-незамещенных диазиридинов оксидом серебра. Для получения 3-хлородиазиринов обычно используют взаимодействие амидинов с гипохлоритом натрия. [26]
Это вещество имеет совсем иные свойства, чем обычный ( линейный) диазометан. Получается циклодиазометан следующим образом. Формальдегид конденсируется с аммиаком и хлорамином в метаноль-яом растворе, образуя циклическое соединение - диазиридин. [27]
Это вещество имеет совсем чные свойства, чем обычный ( линейный) диазометан. Получается циклодиазометан следующим образом. Формальдегид конденсируется с аммиаком и хлорамином в метаноль-ном растворе, образуя циклическое соединение - диазиридин. [28]
Несмотря на сильно напряженную структуру, ЗЯ-дназнрины удивительно нереакционноспособны. Они не изменяются при действии щелочей и в отличие от диазоалканов не взаимодействуют с кислотами или другими элсктрофилышми реагентами. Они вступают, однако, в реакцию с гриньяровскими реагентами при О С, давая 1-замещенные диазиридины. Сходным образом присоединяются и другие металлоорганические реагенты. Напротив, при действии сильных восстанавливающих агентов диазиридины образуются только как трудно выделяемые интермедиаты, поскольку процесс сопровождается дальнейшим восстановлением с раскрытием цикла и образованием аммиака и аминов. [29]
Максимально ограничена конформационная свобода в диазиридинах: здесь приходится делать выбор лишь между цил - и гра с-расположение. ФЭС позволяют однозначно определить конформацию. По причинам как стерическим, так и взаимодействия неподеленных пар, преобладать должна г / го - конформация. Не эмпирические расчеты [76] дают для самого диазиридина преимущественно T / ww - формы в 34 кДж / моль. Угол 102, определенный для 1, 2-диметилдиазиридина в работе [ 491, совпадает с определенным для тетраалкилгидразинов ( табл. 2), что указывает на оптимальное расположение неподеленных пар в транс-форме. [30]
Страницы: 1 2 3