Аммиакат - кобальт
Cтраница 3
Реакции комплексообразования могут изменять потенциал системы. Так, аммиакат кобальта ( II) на воздухе быстро переходит в аммиакат кобальта ( III), так как последний значительно устойчивей. [31]
Сульфит аммония ( NH4) 2S03 в водном растворе кислородом воздуха медленно окисляется до сульфата. В присутствии комплексных, аммиакатов кобальта, как установил Форлендер ( Vorlander, 1930), реакция настолько ускоряется, что ее можно использовать в технике для получения азота из воздуха и одновременно сульфата аммония. [32]
В литературе приведены данные ряда измерений скорости реакций, показывающих, что различные цис - и транс-изомеры [ которые во многих случаях выделены, в частности для комплексов кобальта ( III) ] медленно переходят один в другой и в другие комплексы; пока ни одна система втого типа полностью не изучена. Автор считает, что замещенные обменными реакциями аммиакаты кобальта ( III) обычна перестраиваются самыми различными путями, как будта только малые различия энергии ( обусловленные взаимным расположением лигандов) определяют ту или иную конфигурацию. [33]
В литературе приведены данные ряда измерений скорости реакций, показывающих, что различные цис - и транс-изомеры [ которые во многих случаях выделены, в частности для комплексов кобальта ( III) ] медленно переходят один в другой и в другие комплексы; пока ни одна система этого типа полностью не изучена. Автор считает, что замещенные обменными реакциями аммиакаты кобальта ( III) обычно перестраиваются самыми различными путями, как будто только малые различия энергии ( обусловленные взаимным расположением лигандов) определяют ту или иную конфигурацию. [34]
 |
Частоты связи Pt-H ( в смГ1 в комплексах ( 3R3 2PtHX. [35] |
Совсем недавно А. В. Аблову и Н. М. Самусь Зо как будто удалось найти объяснение, на первый взгляд, странному различию в величине mpawc - влияния роданогруппы в аммиакатах и диоксиминах кобальта. Дело в том, что роданогруппа в аммиакатах кобальта связана с металлом через азот, а в диоксиминах - через серу. Даже независимо от данного частного случая это очень интересно, так как, очевидно, величина транс-влияния сложных заместителей должна зависеть от способа их прикрепления к центральному атому. [36]
Совсем недавно А. В. Аблову и Н. М. Саыусь 30 как будто удалось найти объяснение, на первый взгляд, странному различию в величине транс-влияния роданогруппы в аммиакатах и диокснминах кобальта. Дело в том, что роданогруппа в аммиакатах кобальта связана с металлом через азот, а в диоксиминах - через серу. Даже независимо отданного частного случая это очень интересно, так как, очевидно, величина транс-влияния сложных заместителей должна зависеть от способа их прикрепления к центральному атому. [37]
Реакции комплексообразования могут изменять потенциал системы. Так, аммиакат кобальта ( II) на воздухе быстро переходит в аммиакат кобальта ( III), так как последний значительно устойчивей. [38]
Для синтеза [ Co ( NH3) 5Cl ] Cl2 10 г карбоната кобальта растворить в малом количестве НС1 ( 1: 2), раствор отфильтровать и к фильтрату прибавить 125 мл концентрированного раствора аммиака и раствор, содержащий 50 г хлорида аммония в 125 мл воды. Во время окисления образуются [ Со ( МН3) 5С1 ] С12 и другие аммиакаты кобальта. [39]
Во время окисления происходит образование [ Со ( МН3) 5С1 ] С12 и других аммиакатов кобальта. [40]
Так, например, считалось, что хлорид кобальта имеет состав СогС1в по аналогии с FeaCle; отсюда аммиакаты кобальта принимались димерными. [41]
В колонку вносят три капли раствора смеси катионов Со2 1 и Ni2; хроматограмму проявляют пятью каплями концентрированного раствора аммиака. Сначала вверху появляется розовая зона ( ионы кобальта), постепенно желтеющая, так как Со2 переходит в Со3 ( образование аммиаката кобальта), а внизу-голубая зона аммиаката никеля. [42]
В противоположность этим цианидным ионам, аммиакаты железа совсем неустойчивы. Например, ион [ Fe ( NH3) 6 ] 2 - разлагается водой, а трехвалентное железо не образует аммиакатов, сравнимых по своей устойчивости с аммиакатами кобальта. [43]
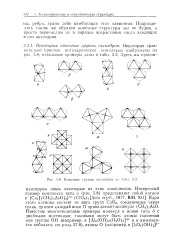 |
Конечные группы октаэдров in. [44] |
Интересный пример комплекса типа а ( рис. 5.8) представляет собой катион в Са2 [ ( СН3) зАзО ] 9 4 ( C104) 4 [ Acta cryst. Известны многочисленные примеры молекул и ионов типа б с двойными мостиками; таковыми могут быть атомы галогенов или группы ОН ( например, в [ Al2 ( OH) 2 ( H2O) 8 ] 4 и в аммиакатах кобальта; см. разд. [45]
Страницы: 1 2 3 4