Елович
Cтраница 2
В 1934 г. Зельдович [33] вывел уравнение, которое впоследствии было использовано Еловичем [34] и другими для того, чтобы выразить сложные адсорбционные явления в общем виде. [16]
Уместно рассмотреть вопрос, почему хемосорбция кислорода не менее чем на трех из этих окислов подчиняется уравнению Еловича. [17]
Второе предположение подтверждается тем, что, как было ранее показано, оно находится в согласии с уравнением Еловича. Однако любая другая лимитирующая стадия хемосорбции кислорода, энергия активации которой зависит от степени заполнения поверхности в соответствии с уравнением Еловича, также согласуется с этими данными. [18]
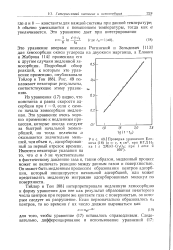 |
Проверка уравнения Ело. [19] |
Это уравнение впервые описали Рогинский и Зельдович [ ИЗ ] для хемосорбции окиси углерода на двуокиси марганца, а Елович и Жаброва 114 ] применили его к другим случаям медленной хемосорбции. [20]
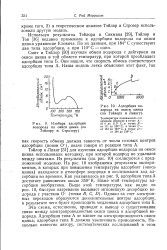 |
Изобара адсорбции. [21] |
Используя результаты Тэйлора и Сикмана [29], Тэйлор и Тон [36] недавно применили к адсорбции водорода на окиси цинка уравнение Еловича. По их данным, при 184 С существуют два типа адсорбции, а при 110 С - один. [22]
Ряд рекомендаций по предупреждению отравлений Hg в условиях производства приведен в работах Богатыревой; Быховского и Найденко; Гимаде-ева; Тученко и Елович; Евентовой и Коган; Пьянкова; Склянской-Василев - ской. Мероприятия по профилактике меркуриализма регламентируются специальными постановлениями. Приводим ниже перечень ряда этих документов. [23]
Ряд рекомендаций по предупреждению отравлений Hg в условиях производства приведен в работах Богатыревой; Выховского и Найденко; Гимаде-ева; Тученко и Елович; Евентовой и Коган; Пьянкова; Склянской-Василев - ской. Мероприятия по профилактике меркуриализма регламентируются специальными постановлениями. Приводим ниже перечень ряда этих документов. [24]
Скорости этих медленных процессов хемосорбции часто подчиняются наиболее интересному из известных в настоящее время кинетических законов ( в интегрированной форме) - уравнению Еловича. [25]
Адсорбция кислорода на некоторых окислах превышает монослойную; первая часть хемосорбции быстрая, а более поздние стадии по заполнении монослоя медленные, соответствующие уравнению Еловича. [26]
В литературе не имеется никаких стадийных схем окисления углеводородов на других металлических контактах, за исключением схемы окисления пропилена на платине, предложенной Бутягиным и Еловичем [ 15 J. По этой схеме в результате взаимодействия углеводорода с кислородом, адсорбированным на катализаторе, образуется первое промежуточное соединение углеводорода с кислородом. При дальнейшем окислении этого соединения возможны два пути реакции в зависимости от температуры. При низких температурах наблюдается поверхностное, а при высоких температурах - поверхностно-объемное окисление. Последний процесс представляет собой десорбцию неустойчивого ( по отношению к кислороду) промежуточного соединения, образующегося на катализаторе, в объем. В газовой фазе это соединение реагирует с кислородом и образуются углекислый газ и вода. [27]
Кинетика хемосорбции кислорода с образованием функциональных групп исследована в целом ряде работ, например [150-152], и показано, что она может быть описана уравнениями типа соотношения Еловича. К сожалению, в литературе отсутствуют данные по адсорбции кислорода в условиях стационарного заполнения поверхности углеродных материалов функциональными группами. Именно эти результаты могли бы быть непосредственно сопоставлены с данными по электрокатализу. [28]
С точки зрения модели Марса - Ван Кревелена, очень важно знать, какой процент атомов кислорода на поверхности в действительности принимает участие в каталитическом окислении. Васильев, Елович и Марголис [57] и Боресков [58] показали, что поверхности многих окислов энергетически неоднородны. Это подтверждается следующими фактами. Небольшой процент поверхностного кислорода может обмениваться с газообразным кислородом с исключительно низкой энергией активации. Энергия активации растет с увеличением степени кислородного обмена. Поскольку образцы Ройтера подвергались обработке в вакууме при 500 или 550 С, вероятно, наиболее лабильный кислород был уже удален еще до того, как были начаты изотопные эксперименты. [29]
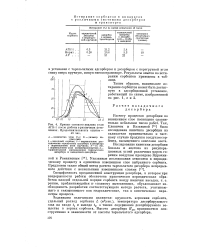 |
Кривые ситового анализа угля АГК-1 после работы в различных установках. Продолжительность опытои - 48 час. [30] |
Страницы: 1 2 3 4