Мильнер
Cтраница 2
Первая успешная попытка объяснить отклонение электролитов от идеального поведения была сделана Мильнером в 1912 г., однако его теория была очень сложна. Представления Мильнера в сущности совпадают со взглядами, которые были развиты в более доступной форме Дебаем и Гюккелем. Основные положения их теории уже были изложены на стр. [16]
Элементарная модель языка LOTOS основывается на исчислении взаимодействующих систем [7], разработанном Мильнером. В свою очередь исчисление взаимодействующих систем ( ИВС) включает небольшое множество примитивных понятий. Хотя в дальнейшем сохраним введенную уже терминологию гл. ИВС носит название агента, а оператор - комбинатора. Комбинаторы [ ИВС ( операторы языка LOTOS) служат для построения новых агентов ( процессов) из уже существующих и выбраны так, чтобы не только выполнять такие построения, но и чтобы отношение между поведениями нового и исходного агентов ( процессов) можно было трактовать в математическом смысле. [17]
Как было показано, существует множество различных экспериментальных данных, подтверждающих основной вывод Мильнера о том, что свободная энергия растворов электролитов при сильном разбавлении пропорциональна квадратному корню из общей ионной концентрации. При этом коэффициент пропорциональности зависит только от ионной силы, температуры и диэлектрической постоянной среды и, следовательно, не содержит каких-либо специфических коэффициентов. Этим, безусловно, объясняется та большая популярность, которой эта теория пользуется среди экспериментаторов. Такое хорошее согласие, которое показано в табл. 28, как правило, ограничивается растворами, содержащими не более одного миллимоля электролита it литре. Это вызвало неуместные и явно несправедливые замечания о том, что теория сильных электролитов с учетом межионного взаимодействия является не более как теорией слабо загрязненной воды. Признавая правильность основных положений теории и трудности ее математического аппарата, нельзя упускать из виду и ее недостатков, проявляющихся даже и случае высоких разбавлении. Так, например, только 4 из 18 электролитов, приведенных в табл. 3, имеют электропроводность с отклонением в пределах 10 % от теоретически требуемой величины. Более того, теория совершенно не дает оценки абсолютных значений свойств ионов при бесконечном разбавлении, а имеет дело лишь-с тем, как изменяются эти величины с концентрацией при разбавлениях, близких к бесконечному. Теория сольватации ио Борну, подобно объяснению Вальденом значений Лео в различных растворителях, является определенным шагом в этом направлении. Изложение теории ионных растворов с выводом уравнения ( 89) представляет собой попытку объединить важнейшие идеи Мильнера и Борна на общей основе. [18]
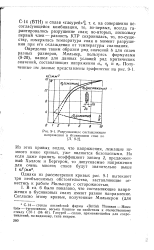 |
Разрушающие составляющие. [19] |
Однако из рассмотрения кривых рис. 9 - 1 вытекают три необъяснимых обстоятельства, заставляющие отнестись к работе Мильнера с осторожностью. [20]
Всю задачу можно решить и более непосредственно, рассматривая не ионные атмосферы, но взаимодействие точечных зарядов отдельных ионов, что сделали Мильнер ( 1912), Ф аул ер ( 1927) и Крамере ( 1928), однако такие расчеты очень сложны и могли быть сделаны до конца лишь для простейших случаев. [21]
Представляется естественным, что теории растворов электролитов при обычных концентрациях должны бы в значительной степени основываться на попытках распространения на них теории Мильнера - Дебая, которая как по характеру ее вывода, так и по соответствию с опытными данными имеет силу только для очень разбавленных растворов. [22]
Для описания параллельных процессов применяются алгебраические спецификации, в частности, алгебры процессов, известные как CSP Хоараи CCS ( Calculus of Communicating Systems) Мильнера. [23]
Бьеррум [77] рассматривает ионы типа /, находящиеся на расстояниях, меньших, чем а0, от центрального иона типа г, как ассоциированные, а ионы типа /, удаленные на расстояния, большие, чем а0 - как свободные и подчиняющиеся распределению Мильнера - Дебая. [24]
Фигурные скобки в этом уравнении указывают на то, что приведенные величины являются активностями; их значения легко можно получить, если концентрации ( величины, приводимые в квадратных скобках) настолько малы, что коэффициенты активности зависят только от заряда; они равны единице в случае нейтральных частиц и имеют стандартные значения Дебая - Мильнера для ионов. [25]
Наиболее успешно развивалось теоретическое исследование свойств разведенных растворов электролитов. Мильнер, а затем Дебай и Хюккель предложили теорию, которая, как показала последующая экспериментальная проверка, количественно отображает свойства растворов сильных электролитов при больших степенях разведения. [26]
Титрованный раствор железа многие авторы применяют для обратного титрования. Мильнер и Пеннах [ 54 ( 92) ] проводят обратное титрование при рН 5 - 6 с салициловой кислотой, тогда как Володарская [ 60 ( 93) ] применяет в тех же условиях сульфосали-циловую кислоту. В обоих случаях прибавляют в избытке ЭДТА, рН анализируемого раствора доводят до значения 6 и раствор кипятят одну минуту, затем его охлаждают до 30 С, добавляют ацетатный буферный раствор ( до рН 4) и проводят обратное титрование. [27]
Наиболее успешно развивалось теоретическое исследование свойств разведенных растворов электролитов. Мильнер, а затем Дебай и Хюккель предложили теорию, которая, как показала последующая экспериментальная проверка, количественно отображает свойства растворов сильных электролитов при больших степенях разведения. [28]
Первая успешная попытка объяснить отклонение электролитов от идеального поведения была сделана Мильнером в 1912 г., однако его теория была очень сложна. Представления Мильнера в сущности совпадают со взглядами, которые были развиты в более доступной форме Дебаем и Гюккелем. Основные положения их теории уже были изложены на стр. [29]
Твердые растворы могут считаться совершенными кристаллическими веществами только в случае некоторых определенных молекул, соответствующим образом расположенных в узлах решетки. Истмэн и Мильнер [166] показали, что энтропия образования твердого раствора [ 73 % AgBr ] из смеси чистых хлористого и бромистого серебра составляет при 298 К 1 12 0 1 кал-град-1 - моль 1 против значения 1 16 кал-град-1 - моль-1, рассчитанного для известного состава. Так как теплоемкость твердого раствора ниже 298 К не сильно отличается от суммы теплоемкостей чистых составляющих, то при 0 К энтропия смешения, вероятно, еще не равна нулю, поэтому можно сделать заключение, что ионы хлора и брома беспорядочно распределены по узлам решетки. [30]
Страницы: 1 2 3 4