Минимум - потенциальная кривая
Cтраница 4
Вообще говоря, электронный переход может произойти из любой точки потенциальной кривой, в какой испытывающая колебания система может оказаться при данной температуре. Однако вероятность перехода зависит от вероятности нахождения системы в состоянии с той или иной координатой, которая в свою очередь выражается гауссовой кривой. Максимум последней отвечает минимуму потенциальной кривой. [46]
 |
Потенциальные кривые Н - связи. Асимметричная нейтральная Н - связь, б и в симметричная ионная И-связь. [47] |
Энергия Н - связи средней прочности для различных комплексов варьирует в пределах 1 - т - 15 ккал / моль, что более чем па порядок превышает энергии связи ван-дер-ваалъсовых диморов и в то же время более чем на порядок меньше энергий химических связей. Длина Н - связи, определяемая как расстояние между атомами X и Y, составляет 2 7 - - 3 0 А, что, если учесть, что между атомами X и Y находится атом Н, существенно меньше равновесных расстояний в ван-дер-ваалъсовых димерах. Положение протона определяется минимумом потенциальной кривой. [48]
Различные случаи распределения интенсивности можно наглядно объяснить с помощью принципа Франка - Кондона. Согласно первоначальной полу классической идее Франка, квантовый скачок из одного электронного состояния в другое происходит очень быстро по сравнению с движением ядер; поэтому сразу же после квантового скачка ни положение ядер, ни их скорость не изменяются. При поглощении, если пренебречь нулевым колебанием, молекула первоначально находится в минимуме нижней потенциальной кривой. Квантовый скачок, обусловленный поглощением кванта света, переводит молекулу на верхнюю потенциальную кривую в точку с тем же значением г и ( приблизительно) нулевой скоростью. В связи с изменением потенциальной кривой молекула теперь начинает осциллировать между точками В и С. [49]
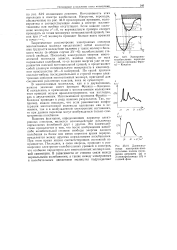 |
Электронно-колебательные переходы с учетом принципа Франка - Кондона.| Длинноволновые электронно-колебательные полосы поглощения антрацена ( а и 3-аминофталимида ( б в газовой фазе. [50] |
Интенсивность этих переходов в спектре наибольшая. Напротив, переходы, обозначенные на рис. 33.9 пунктирными прямыми, маловероятны и соответствующие линии в спектре малоинтенсивны или вообще отсутствуют. Если нижнее состояние молекулы а 0, то вертикальную прямую следует проводить из точки минимума потенциальной кривой, так как при v Q молекула проводит больше всего времени в точке г ге. [51]
Вычисление потенциальных энергий взаимодействия адсорбат-адсорбент на основе полуэмпирических потенциальных функций представляет и самостоятельный интерес. Потенциальная энергия адсорбции молекул при наиболее выгодной ее ориентации на поверхности равна теплоте адсорбции при абсолютном нуле. Вследствие довольно незначительной зависимости теплоты адсорбции при малых заполнениях поверхности от температуры значение потенциальной энергии адсорбции в минимуме потенциальной кривой довольно близко и к теплоте адсорбции при температуре хроматографической колонны. [52]
В случае, показанном на рис. 2 - 8, б, переходы менее вероятны. Для случая, показанного на рис. 2 - 8, в, разрешенные переходы могут привести к диссоциации молекулы при условии, что колебательный уровень, на который происходит переход, лежит выше предела диссоциации. Молекулу, содержащую атом, для которого возможен изомерный переход, можно рассматривать, как находящуюся в состоянии /, соответствующем минимуму потенциальной кривой. После изомерного перехода и электронной перегруппировки новое электронное состояние может соответствовать потенциальной кривой, подобной кривой / / ( рис. 2 - 8, в); при возбуждении колебаний в этом случае будет происходить диссоциация. [53]
С-С - связи как бы затормаживается. Поэтому конформации, соответствующие минимумам кривой потенциальной энергии, паз. Переход от максимума к минимуму энергии осуществляется поворотом оси С-С на 60, поэтому для молекулытипа НЧРНЗС-GR4H6R6 мыслимы три различные конформации, отвечающие минимумам потенциальной кривой. Если нек-рые из заместителей одинаковы, то и нек-рые из конформации эквивалентны и число их сокращается. [55]
В работах [174, 175] молекулярно-статистическим методом были рассчитаны термодинамические характеристики адсорбции бензола, нафталина, антрацена и фенантрена на базисной грани графита. Параметры функций ф оценивались исходя из свойств адсорбата и адсорбента, взятых в отдельности. Значения Ф0 - потенциальной энергии адсорбции в минимуме потенциальной кривой - для антрацена и фенантрена принимались одинаковыми. [56]
Поскольку конфигурационное разложение является сходящимся, расчет тем точнее, чем больше число учитываемых конфигураций, к тому же конфигурационный ряд па хартри-фоковских орбиталях сходится очень медленно. Современные вычислительные машины позволяют проводить расчеты с учетом громадного количества конфигураций. В качестве примера приведем расчет димера воды Дирксена с соавторами [96], в котором использовалась вариационная функция, содержащая 56 268 однократно и двухкратно возбужденных конфигураций. Согласно полученным результатам, абсолютное значение энергии корреляции, как и следовало ожидать, падает с увеличением расстояния между молекулами. В точке минимума потенциальной кривой корреляционная поправка к энергии связи составляет 1 03 ккал / молъ, или - 16 % от полной энергии связи димера. Помимо значительного увеличения энергии связи, учет электронной корреляции приводит к небольшому уменьшению равновесного расстояния: от До-о - 3 00 А при расчете по методу ССП МО ЛКАО до Д () - о 2 919 А при учете конфигурационного взаимодействия. [57]
Изучение вещества, состоящего из разнородных атомов, приводит к представлению об ионной или гетерополярной связи; типичным примером такого вещества может служить NaCl. Один валентный электрон натрия переходит к атому хлора. Кулоновские силы притяжения уравновешиваются силами отталкивания; последние возникают, когда электронные оболочки ионов начинают перекрывать друг друга. Многие свойства простых ионных соединений можно объяснить, исходя из теории Борна и представителей его школы. Поэтому разность между максимумом и минимумом потенциальной кривой в данном случае значительно больше, чем в кристаллах с ковалентной или металлической связью; в результате в ионных соединениях запретная зона широка. Измерение значений подвижности носителей в кристаллах с низкой электропроводностью представляет значительные трудности, и в литературе по этому вопросу имеется немного экспериментальных данных. [58]
Уровни представлены горизонтальными линиями. Колебание имеет место во всем диапазоне г, где V ( г) меньше, чем энергия уровня. Наинизший колебательный уровень имеет конечную величину и, следовательно, энергию jffinne минимума потенциальной кривой, что является характерной чертой квантовой теории. [59]
 |
Схема роста цепи на двухбуквенной матрице ( звездочкой помечен активный конец цепи. [60] |
Страницы: 1 2 3 4 5
