Мирицетин
Cтраница 2
Эггер и Кейл [352] в 1965 г. опубликовали работу по разделению большого числа гликозидов таких агликонов, как кемпферол, кверцетин и мирицетин, отличающихся друг от друга числом гидроксильных групп. При этом было обнаружено два явления, не объяснимых с точки зрения представлений об адсорбции на полиамиде. Во-первых, в системе метанол-вода производные мирицетина продвигаются быстрее, чем соответствующие гликозиды кверцетина и кемпферол а, и, во-вторых, глюкозиды продвигаются быстрее рамнозидов. [16]
Недавно было описано [ 1721 разделение на тонком слое полиамидного порошка перлона 14 гликозпдов, у которых аглюкоиамн были кэмпферол, кверцетпн и мирицетин, а в углеводную часть включались рамноза, арабиноза, глюкоза и галактоза. [17]
Эггер и Кейл [ 3521 в 1965 г. опубликовали работу по разделению большого числа гликозидов таких агликонов, как кемпферол, кверцетин и мирицетин, отличающихся друг от друга числом гидроксильных групп. При этом было обнаружено два явления, не объяснимых с точки зрения представлений об адсорбции на полиамиде. Во-первых, в системе метанол-вода производные мирицетина продвигаются быстрее, чем соответствующие гликозиды кверцетина и кемпферола, и, во-вторых, глюкозиды продвигаются быстрее рамнозидов, С позиций адсорбции, учитывающей количество гидроксильных групп, можно было бы ожидать как раз обратное явление. Авторы [352] пришли к убеждению, что при хроматографирова-нии в системе метанол-вода, более полярной, чем полиамид, имеет место распределительный процесс. При применении растворителей элюотропного ряда влияние заместителей ( гидрок-еильных групп) в молекуле флавоноида на процессы распределения и адсорбции противоположно. Поэтому в целях более эффективного разделения необходимо совместить направления этих двух процессов. Для этого нужно перейти к растворителю менее полярному, чем полиамидная поверхность. В целом, Эггер и Кейл [352] делают вывод, что в липофильных растворителях ( например, хлороформ-метанол-метилэтилкетон, 9: 4: 2) флавоноидные соединения разделяются на полиамиде преимущественно по распределительному механизму. [18]
При помощи хроматографии на бумаге в листьях скумпии обнаружено не менее девяти веществ фенольного характера, из которых галловая кислота и два флавоноида - мирицетин - ( 3) - О-а - Ь - рамнофураноз ид, [ Гпл. Третий фла-воноидный гликозид присутствует в незначительном количестве. [19]
Изучалось влияние ряда веществ флавоноидной природы на структурное состояние различных биомембран, включая мембраны тканей различных сосудов, а также проведено фармакокинетическое исследование кверцетина, мирицетина, гиперозида и байкалина. [20]
Кверцетин находится в розах совместно с цианидином, а Эверест нашел в темно-пурпурных анютиных глазках ( Suttons black knight) наряду с производным дельфи-нидина - виаланином, также флавонол - мирицетин. Восстановлением коерцетина Эверест получил красящее вещество, соответствующее по спектроскопическим данным цианидину, а Схибата и потом Схибата и Казиваги получили из мирицетина хлорид дельфинидина. [21]
Получаемый таким путем из листьев чая препарат ( витамин Р) состоит из свободных катехинов, ближайших продуктов их уплотнения, малых количеств флавонолов ( гликозиды кемпферола, кверцетина и мирицетина) и примесей хлорофилла. Препарат обладает высокой капилляроукрепляющей активностью и применяется в медицинских учреждениях перорально в виде порошка или таблеток. Для целей парентерального введения препарат подвергается дополнительной очистке. [22]
Оно присутствует с удивительным постоянством в группе Myrtinae из Myrtiflorae, причем оно найдено во всех девяти семействах и в большинстве проверенных видов ( из 28 родов) вместе с родственными веществами - мирицетином и лейкодельфинидином. [23]
В предыдущих разделах были обсуждены особенности фармакокинетики флавонгликозидов и агликонов, а также влияние остатка сахара у гиперозида на объем распределения и время удержания лекарственного вещества в организме животного по сравнению с флавоноида-ми агликонами кверцетином и мирицетином. В этом контексте байкалин является флавоноидом с более усложненной структурой, т.к. кроме остатка сахара имеет остаток глюкуроновой кислоты, за счет которого способен образовывать комплексы со многими фрагментами белков и липидов мембран клеток крови и тканей. [24]
По-видимому, в гидролизатах присутствуют следующие типы соединений: флуоресцирующие вещества в солянокислых экстрактах озерных осадков и торфа, выделенные методом бумажной хроматографии; рибофлавин, рибофлавин фосфат и другие производные желтых энзимов или флавопротеинов, включающие мирицетин, люмифлавин и флавинаденин-динуклеотид ( фад); производные индола и триптофана, включая кинуренин и оксиантраниловую кислоту; производные алкалоида, возможно, включающие никотиновые соединения; порфирины, например, этиопорфирин. [25]
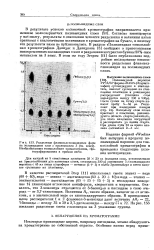 |
Разделение флавонолглюкозидных форм на полиамидном слое с проявителем 3 ( текст. Необработанная тонкослойная хроматограмма, сфотографированная в прямом свете. [26] |
В качестве растворителей Эгер [11] использовал смеси этанол - вода ( 60 40), вода - этанол - ацетилацетон ( 40 20 10) и вода - этанол - этилметилкетон - ацетилацетон ( 65 15 15 5) и исследовал поведение 14 глюкозидов аглюконов кемпферола, кверцетина и мирицетина. Оказалось, что 3-монозиды отделяются от 3-биозидов и последние в свою очередь - от 3 7-глюкозидов. Величины Rf, таким образом, зависят не от аглю-кона, а в значительной мере от глюкозидируемого образца. На рис. 153 показано разделение смеси глюкозидов на 3 указанные группы. [27]
 |
Разделение флавонолглюкозидных форм на полиамидном слое с проявителем 3 ( текст. Необработанная тонкослойная хроматограмма, сфотографированная в прямом свете. [28] |
В качестве растворителей Эгер [11] использовал смеси этанол - вода ( 60 40), вода - этанол: - ацетилацетон ( 40 20 10) и вода - этанол - этилметилкетон - ацетилацетон ( 65 15 15 5) и исследовал поведение 14 глюкозидов аглюконов кемпферола, кверцетина и мирицетина. Оказалось, что 3-монозиды отделяются от 3-биозидов и последние в свою очередь - от 3 7-глюкозидов. Величины Rf, таким образом, зависят не от аглю-кона, а в значительной мере от глюкозидируемого образца. На рис. 153 показано разделение смеси глюкозидов на 3 указанные группы. [29]
Антиоксидантную активность проявляют многие флавоноиды, в том числе мирииетин и дигидрокверцетин. Активность этих соединений уменьшается от мирицетина к кверцетину, рамнентину, морину, диосме-тину, нарингенину, апигенину, катехину, робинину, кемферолу и флаво-ну. [30]
Страницы: 1 2 3 4