Предэкспоненциальный множитель - константа - скорость
Cтраница 1
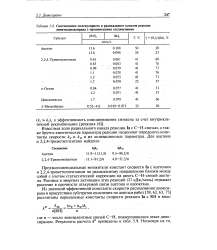 |
Соотношение молекулярного и радикального каналов реакции диметилдиоксирана с органическими соединениями. [1] |
Предэкспоненциальные множители констант скорости Та с ацетоном и 2 2 4-триметилпентаном по радикальному направлению близки между собой с учетом статистической коррекции на шесть С - Н - связей ацетона. Разница в энергиях активации этих реакций ( 21 кДж / моль) отражает различие в прочности атакуемой связи ацетона и изооктана. [2]
Предэкспоненциальный множитель константы скорости изомеризации в комплексе ( С R) имеет значение, характерное для обычных мономолекулярных реакций. [3]
Расчет предэкспоненциального множителя константы скорости может быть произведен с помощью выражений статистической механики для сумм состояний [ см. уравнения (1.69) и (1.70) ], при выборе определенной модели активированного комплекса и справочных величин - для масс молекул, моментов инерции и частот колебаний исходных веществ. [4]
На рис. 7 - 13 представлены экспериментальные значения предэкспоненциального множителя констант скорости диссоциации для ряда молекул, диссоциирующих в среде аргона. [5]
Естественно предположить, что такое несоответствие обусловлено одновременным изменением предэкспоненциального множителя константы скорости реакции, которое компенсирует резкие изменения экспонента. Такое явление обычно называют компенсационным эффектом [706] и некоторые авторы придают ему большое значение. Гиншельвуд [724] признает компенсационный эфф ект одной из основных, хотя и непонятных, закономерностей химической кинетики. [6]
Авторами теоретически было найдено, что в области низких температур предэкспоненциальный множитель константы скорости реакции первого порядка имеет положительную температурную зависимость, а при высоких температурах показатель степени зависимости от температуры может стать отрицательным или нулевым. [7]
Как мы уже указывали, для такого типа реакций мало различаются предэкспоненциальные множители констант скоростей. Если же реакции развития цепи состоят из стадий, включающих не только реакции замещения, но и реакции присоединения, то в этих случаях для определения наиболее медленной стадии необходимо учитывать различие не только в энергиях активации, но и в стерических факторах. Мы видели в главе I, что реакции присоединения атомов или радикалов к двойной связи идут замедленно вследствие очень малых, в сравнении с реакциями замещения, стерических факторов. [8]
 |
Энергии разрыва связей R - H. [9] |
С увеличением ее прочности энергия активации реакции снижается и, так как предэкспоненциальные множители констант скорости реакции замещения различных радикалов можно считать в первом приближении одинаковыми, энергия разрыва связи R - Н может служить мерой активности радикала R - в реакциях замещения. В табл. 1.7 приведены энергии связи некоторых радикалов с атомом водорода в порядке возрастания прочности связи и, следовательно, активности радикалов в реакциях замещения. [10]
Каков бы ни был механизм миграции, можно показать, что значения предэкспоненциального множителя константы скорости k должны быть в пределах 10 9 - 10 14 см3 / сек, а энергия активации составлять менее 20 - 30 ккал / молъ. Однако экспериментальные значения k и Ez часто не совпадают с указанными значениями; наблюдаются значения k % до 10 см3 / сек, а Е2 достигает 60 ккал / молъ, хотя абсолютные значения констант &2 имеют разумные значения, а между g k и Ez для сходных полимеров наблюдается компенсационная линейная зависимость. В работах 71 72 было показано, что этот эффект может быть объяснен неприменимостью соотношения Аррениуса к реакциям в твердой фазе; причина неприменимости заключается в том, что значения истинных энергий активации уменьшаются с ростом температуры. [11]
Каков бы ни был механизм миграции, можно показать, что значения предэкспоненциального множителя константы скорости й должны быть в пределах 10 9 - 10 14 см9 / сек, а энергия активации составлять менее 20 - 30 ккал / молъ. Однако экспериментальные значения & S и Ег часто не совпадают с указанными значениями; наблюдаются значения k до 10 6 см9 / сек, а Е % достигает 60 ккал / молъ, хотя абсолютные значения констант Л2 имеют разумные значения, а между lg k и Е2 для сходных полимеров наблюдается компенсационная линейная зависимость. В работах71 72 было показано, что этот эффект может быть объяснен неприменимостью соотношения Аррениуса к реакциям в твердой фазе; причина неприменимости заключается в том, что значения истинных энергий активации уменьшаются с ростом температуры. [12]
Возможность нахождения статистических сумм и позволяет воспользоваться методом переходного состояния для расчетов предэкспоненциальных множителей констант скоростей реакций. [13]
Если этот механизм верен, то для первой стадии, определяющей скорость, предэкспоненциальный множитель константы скорости составляет 6 - 10 см31моль - сек, а энергия активации в интервале - 80 -: - 20 С равна 1 5 ккал / моль. [14]
А и X; E и Е2 - энергии активации; zl и za - предэкспоненциальные множители констант скорости 1 - й и 2 - й реакций; Qz - тепловой эффект 2 - й реакции; с - объемная теплоемкость смеси; Т - ее температура; Тй - температура стенки реактора; S и V - его поверхность и объем; а - коэффициент теплопередачи; R - газовая постоянная; t - время. [15]
Страницы: 1 2 3