Предэкспоненциальный множитель - константа - скорость
Cтраница 2
В связи с этим диссоциация через образование комплекса не может быть привлечена для объяснения отрицательной температурной зависимости предэкспоненциального множителя константы скорости распада двухатомных молекул при высоких температурах. [16]
А; Хд - Степень превращения по реагенту А; Е, Е2 - энергия активации соответственно для прямой и обратной реакций; &01, йог - предэкспоненциальные множители констант скоростей прямой и обратной реакций; R - универсальная газовая постоянная; Т - абсолютная температура. [17]
 |
Зависимость Д5 от чи. [18] |
Таким образом, все приведенные выше данные показывают, что стабильные радикалы являются удобным инструментом исследования реакционной способности молекул, радикалов и связей и позволяют изучить влияние строения на энергию активации и предэкспоненциальные множители констант скоростей, исследовать роль энергетических и стерических факторов в кинетике. [19]
ОАО - начальная концентрация исходного реагента Л; ХА - степень превращения по реагенту А; Е, Е2 - энергии активации соответственно для прямой - и обратной реакций; k0i, & о2 - предэкспоненциальные множители констант скоростей прямой и обратной реакций; R - универсальная газовая постоянная; Т - абсолютная температура. [20]
При 700 К такое различие в энергии активации дает преимущество цепной реакции примерно в 34 раза. Предэкспоненциальный множитель константы скорости реакции, как мы видели выше, в случае цепной реакции ( при давлениях, близких к атмосферному) примерно в 100 раз меньше предэкспоненциального множителя константы скорости простого мономолекулярного распада. [21]
Рассмотрение конкуренции реакций непосредственного и цепного образования галоидоводородов было облегчено тем, что, во-первых, нам была известна минимальная граница энергии активации Е непосредственной реакции галоида с водородом, во-вторых, обе элементарные стадии цепной реакции являются бимолекулярными реакциями замещения. Для таких реакций предэкспоненциальные множители констант скоростей не сильно различаются, и поэтому наиболее затрудненной стадией цепного процесса оказывается стадия, протекающая с наибольшей энергией активации. [22]
Рассмотрение конкуренции реакций непосредственного и цепного образования галоидоводородов было облегчено тем, что, во-первых, нам была известна минимальная граница энергии активации Е непосредственной реакции галоида с водородом, во-вторых, обе элементарные стадии цепной реакции являются бимолекулярными реакциями замещения. Для таких реакций предэкспоненциальные множители констант скоростей не сильно различаются, и поэтому наиболее затрудненной стадией цепного процесса оказывается стадия, протекающая с наибольшей энергией активации. [23]
Из изложенного вытекают пути расчетов абсолютных скоростей реакций методом переходного состояния. Эти расчеты сводятся к вычислению величин предэкспоненциальных множителей константы скорости соответствующей элементарной реакции. Величины энергии активации в принципе доступны квантовохимической оценке, и подобные расчеты могут рассматриваться как другая сторона приложения теории абсолютных скоростей реакций. [24]
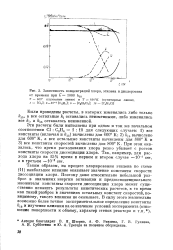 |
Зависимость концентраций хлора, этилена И дихлорэтана от времени при к 1000 к1ъ. [25] |
Таким образом, на процесс хлорирования этилена по схеме ( 11) наибольшее влияние оказывает значение константы скорости диссоциации хлора. Поэтому даже относительно небольшой разброс в значениях энергии активации и предэкспоненциального множителя константы скорости диссоциации хлора может существенно исказить результаты кинетических расчетов, в то время как такой разброс в значениях остальных констант скоростей, по-видимому, такого влияния не оказывает. [26]
При этом в первом приближении принимается, что различия каталитической активности элементарных мест поверхности обусловлены разными значениями энергии активации, но не предэкспоненциальных множителей константы скорости. Это предположение означает одинаковость энтропии активации на всех местах поверхности. [27]
Современная практика ставит также перед теорией новые задачи, решение которых связано с детальным изучением роли разных видов внутримолекулярного движения и различных процессов передачи энергии при столкновениях в кинетике мономолекулярного распада. Важным разделом этой проблемы является, в частности, последовательный учет ограничений, налагаемых сохранением вращательного момента на спонтанный распад молекул и связанное с этим уточнение предэкспоненциального множителя константы скорости мономолекулярного распада в пределе высоких и низких давлений. [28]
При 700 К такое различие в энергии активации дает преимущество цепной реакции примерно в 34 раза. Предэкспоненциальный множитель константы скорости реакции, как мы видели выше, в случае цепной реакции ( при давлениях, близких к атмосферному) примерно в 100 раз меньше предэкспоненциального множителя константы скорости простого мономолекулярного распада. [29]
Как видим, вопрос о том, протекает ли реакция непосредственно по стехиометрическому уравнению или же по цепному механизму, решается просто. Однако такое простое решение возможно лишь в тех случаях, когда цепь состоит из бимолекулярных элементарных стадий, являющихся реакциями замещения радикалов молекулами. Предэкспоненциальные множители констант скоростей этих реакций мало различаются. В-иных случаях следует принимать во внимание и стерические сопротивления. В большой степени это относится к реакция 1 присоединения атомов или радикалов по месту двойной связи. Наиболее медленно идущей реакцией может оказаться реакция присоединения по месту двойной связи не вследствие высокой энергии активации, а вследствие малого стерического коэффициента. [30]
Страницы: 1 2 3