Предэкспоненциальный множитель - константа - скорость
Cтраница 3
Теплота реакции 1) в случае ызо - С3Н7Вг равна - 9 ккал, в случае нормального пропйлбромида 3 ккал, а в случае этилбромида - 3 ккал. При 700 К такое различие в энергии активации дает преимущество цепной реакции примерно в 34 раза. Предэкспоненциальный множитель константы скорости реакции, как мы видели выше, в случае цепной реакции ( при давлениях, близких к атмосферному) примерно в 100 раз меньше предэкспоненциального множителя константы скорости простого мономолекулярного распада. [31]
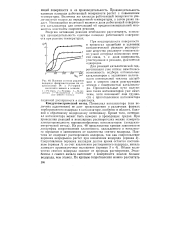 |
Влияние степени удаления водорода фенилацетиленом на сопротивление Pt - и Pd-черней и. [32] |
Производительность единицы площади работающей поверхности растет с повышением температуры. Величина же площади работающей поверхности увеличивается только до определенной температуры, а затем резко падает. Меняющейся величиной является доля работающей поверхности катализатора или отвечающий ей предэкспоненциальный множитель константы скорости реакции. [33]
При повышении температуры вследствие каких-то фазовых переходов в структуре микрорайонов этот потенциальный барьер снижается и рекомбинация радикалов облегчается. Именно при таких температурах и протекает с измеримой скоростью большинство реакций рекомбинации алкильных радикалов. Вследствие этого скорость реакции рекомбинации очень сильно растет с температурой, что приводит на опыте к эффекту увеличения измеряемых энергий активаций и предэкспоненциальных множителей констант скоростей. [34]
Теплота реакции 1) в случае ызо - С3Н7Вг равна - 9 ккал, в случае нормального пропйлбромида 3 ккал, а в случае этилбромида - 3 ккал. При 700 К такое различие в энергии активации дает преимущество цепной реакции примерно в 34 раза. Предэкспоненциальный множитель константы скорости реакции, как мы видели выше, в случае цепной реакции ( при давлениях, близких к атмосферному) примерно в 100 раз меньше предэкспоненциального множителя константы скорости простого мономолекулярного распада. [35]
Абсолютную скорость элементарной реакции принципиально можно вычислить с помощью упомянутой теории активированного комплекса. Однако для этого необходимо посредством методов квантовой механики найти поверхность потенциальной энергии реагирующей системы. Поскольку для гетерогенных каталитических реакций подобный расчет, как правило, не представляется возможным, в случае этих реакций теория активированного комплекса используется для установления формы закона действующих масс и приближенной оценки предэкспоненциального множителя константы скорости. [36]
Сразу же обращают на себя внимание необычно большие значения предэкспоненциальных множителей и энергий активации, особенно в первых двух константах. Проведенные нами приближенные расчеты показали, что различные сложные кинетические механизмы, приводящие к квазибимолекулярной брутто-реакции, а также учет энтропийного члена могут увеличить предэкспоненциальный множитель не более чем на 5 - 6 порядков. Ошибка при расчете константы скорости по неверному порядку также не превышает указанной величины. С другой стороны, аномально большие значения предэкспоненциальных множителей константы скорости рекомбинации наблюдаются и в других полимерах. [37]
Так, в работе [153] было найдено, что на платине скорость адсорбции двуокиси углерода, протекающей в области высоких температур без энергии активации, составляет лишь небольшую долю той, которая бы соответствовала числу ударов о поверхность. Отсюда был сделан вывод о том, что лишь 0 0001 поверхности платины каталитически активна. Как показал Темкин [108], в таком выводе нет необходимости, поскольку, согласно методу переходного состояния, значение предэкспоненциального множителя константы скорости адсорбции зависит от числа степеней свободы, сохраняемых в активированном комплексе. [38]
Страницы: 1 2 3