Стерический множитель
Cтраница 3
Однако качественно этот вопрос ясен, и следует ожидать, что стерические множители бимолекулярных реакций уменьшаются по мере возрастания сложности реагирующих частиц. Это качественное правило подтверждается данными, приведенными в последующих разделах. [31]
В теории активного комплекса, которая будет рассмотрена ниже, даются методы расчета стерического множителя Р с помощью значений молекулярных параметров реагирующей системы. [32]
Полученный результат вполне разумен и в данном случае позволяет сделать вывод о близости стерического множителя единице. Аналогичные результаты получены и для многих других реакций в растворах. [33]
В теории активного комплекса, которая будет рассмотрена ниже, даются методы расчета стерического множителя Р г.. [34]
Полученный результат вполне разумен и в данном случае позволяет сделать вывод о близости стерического множителя единице. Аналогичные результаты получены и для многих других реакций в растворах. [35]
Полученные выражения ( V, 25) и ( V, 26) показывают, что стерическому множителю можно придать вполне определенный смысл. Из уравнений ( V, 25) и ( V, 26) вытекает, что скорость реакции определяется не теплотой активации, а изменением свободно энергии при переходе системы в переходное состояние. Если переход в соответствующее состояние сопровождается большим увеличением энтропии, то, несмотря на большую энергию активации, реакция будет протекать с б ольшой скоростью. [36]
Полученные выражения ( V, 25) и ( V, 26) показывают, что стерическому множителю можно придать вполне определенный смысл. Как будет показано ниже, величины ДО1 и ДЯ связаны с энергией активации, определяемой опытным путем, и, следовательно, множитель, содержащий энтропию активации Д5, соответствует стерическому множителю в теории столкновений. Из уравнений ( V, 25) н ( V, 26) вытекает, что скорость реакции определяется не теплотой активации, а изменением свободной энергии при переходе системы в переходное состояние. Если переход в соответствующее состояние сопровождается большим увеличением энтропии, то, несмотря на большую энергию активации, реакция будет протекать с большой скоростью. [37]
В каком из случаев: при образовании линейного или нелинейного комплекса ( прочие условия одинаковы) - стерический множитель имеет меньшую величину. [38]
Если же в системе протекают две бимолекулярные реакции, одна из которых имеет малую энергию активации и малый стерический множитель, а для другой обе эти величины больше, то повышение температуры будет сказываться еще сильнее. [39]
Сравнивая обе эти теории с простейшей теорией соударений, нетрудно заметить, что различие сводится к тому, что несколько неопределенный стерический множитель Р теории соударений заменяется соотношением ( в принципе более четким) функций распределения частиц А, В и комплекса АВ. [40]
Сравнивая обе эти теории с простейшей теорией соударений, вютрудно заметить, что различие сводится к тому, что несколько неопределенный стерический множитель Р теории соударений заменяется соотношением ( в принципе более четким) функций распределения частиц А, В и комплекса АВ. [41]
Абсолютные значения Р-1 Л ( В) больше экспериментальных ( за исключением реакции 12) в 10 - 103 раз - это соответствует нормальным стерическим множителям. [42]
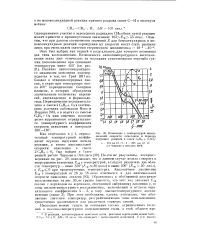 |
Изменение с температурой максимальной скорости окисления и периода индукции реакции в смеси С2Н6 0 502. а - 503 мм рт. ст.. б - 625 мм рт. ст. ( по Чиркову и Энтелису. [43] |
Отметим, что при данном соотношении значений Е для бимолекулярных и мономолекулярных реакций зарождения их скорости могут стать равными лишь при очень малом значении стерического множителя со Ю 5 - Ю 6 Этан был выбран как первый в ряду алканов, для которого возможны два типа воспламенения. Наличие низкотемпературного механизма окисления подтверждается и тем, что Грей [81] наблюдал в этанокислородных смесях, в струе при температуре около 400 периодические холодные пламена, в которых образуются значительные количества перекисей, ацетальдегида и формальдегида. [44]
R - универсальная газовая постоянная ( 8 314 Дж-моль - - К 1); Т - температура, К; Р - так называемый стерический множитель. [45]
Страницы: 1 2 3 4