Энтропийный множитель
Cтраница 1
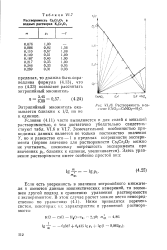 |
Растворимость в системе КХО3 - CsNO3 - Н2О. [1] |
Энтропийный множитель оказывается близким к 1 / 2, но не к единице. [2]
Здесь энтропийный множитель В, равный отношению колебательных сумм состояния, в первом приближении можно не учитывать; A Q Q - v - разность энергий образования соответствующих дефектов на поверхности и в объеме кристалла. [3]
Сравнение энтропийного множителя ( V28) при наличии взаимодействия с соответствующим выражением в случае его отсутствия показывает, что различие между ними не очень большое и иногда им можно пренебречь. [4]
Способы определения энтропийного множителя основаны на растворимости одной соли в водных растворах другой и частично изложены в гл. Но наиболее точным следует признать способ, основанный на уравнении (3.5) гл. [5]
Отсюда следует, что энтропийный множитель не вносит существенного вклада в величину р, так как AS 0, эффект должен определяться знтальпийным множителем. [6]
Этот фактор несколько напоминает энтропийный множитель в выражениях для растворимости [280], объясняющий прекращение набухания и сорбции под влиянием образования пространственной сетки кристаллитов. [7]
Множитель е R в (212.31) называют энтропийным множителем. Он отражает вероятность образования переходного состояния. [8]
Такое соотношение, если оно не компенсируется энтропийным множителем ( что маловероятно), будет вести к обратным изотопным эффектам [204 ] с ускорением, а не замедлением скорости процесса после замещения тяжелым изотопом. Здесь оно будет обусловлено тем, что изотопное замещение приведет к большему снижению величин частот колебаний в активированном комплексе, чем в исходных молекулах. [9]
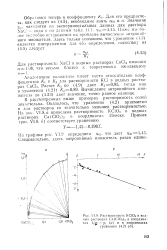 |
Растворимость КСЮ3 в водных растворах Са ( СЮ3 2 в координатах 1 / г - iji ( а и в координатах уравнения ( б. [10] |
Ниже мы более подробно остановимся на проблеме вычисления энтропийного множителя. [11]
Па / ( К-моль), абсолютную температуру Т, энтропийный множитель e s / R, который отражает вероятность образования переходного состояния, а также трансмиссионный коэффициент х, учитывающий возможность распада активированного комплекса на молекулы исходных веществ. В большинстве химических реакций к близок к единице. [12]
Здесь, как и в уравнении (3.22), величина п является энтропийным множителем. [13]
Согласно уравнению ( VIII, 165) стерический фактор называют также энтропийным множителем, или вероятностным фактором. Энтропия активации может быть вычислена при помощи статистической термодинамики, если известно строение активного комплекса. В настоящее время такие расчеты могут быть выполнены только для простейших реакций, так как в большинстве случаев строение активного комплекса неизвестно. [14]
Во всех формулах для вычисления функции распределения по энергиям активации о ( Е) обязательно фигурирует величина энтропийного множителя А0 константы скорости реакции, принимаемая при статистическом анализе неизменной для всей поверхности и определяющая тот интервал значений Е, которому отвечает вычисляемая функция распределения. Аналогичную роль в теории адсорбционного равновесия играет величина Ь0 - энтропийного множителя обратного адсорбционного коэффициента. [15]
Страницы: 1 2 3