Ионная модель
Cтраница 2
В основу ионной модели соединения положено электростатическое взаимодействие ионов. Ионы можно представить как заряженные шары, силовые поля которых равномерно распределяются во всех направлениях в пространстве. Поэтому каждый ион может притягивать к себе ионы противоположного знака в любом направлении. Иначе говоря, ионная связь в отличие от ковалентной характеризуется ненаправленностью. [16]
Очевидно, что ионная модель Берна адекватно передает состояние атомов, по крайней мере в кристаллах галогенидов щелочных металлов, и энергию их взаимодействия в кристаллической решетке. [17]
Латимер [10] для ионной модели рассчитал энтропии атомов свинца и серы при 25 С: s ( РЬрь) 15 5 кал / град и s ( S §) 5 кал / град. [18]
Дополнительным подтверждением правомерности ионных моделей служит, по мнению этих ученых, обычно вполне удовлетворительное совпадение величин энергии кристаллических решеток, полученных из цикла Борна - Габера или рассчитанных по формуле Борна ( 3), основанной на представлениях чисто ионной связи. Например, расчет энергии кристаллической решетки хлорида натрия по формуле Борна дал величину 180 ккал / моль, а экспериментальная величина из цикла Борна - Габера составляет 186 ккал / моль. [19]
 |
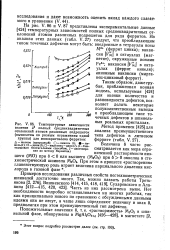
Отношение эффективных зарядов ионов к номинальным в бинарных кристаллах [ 9 - / / ]. [20] |
Наглядным примером условности ионной модели может служить система кристаллохимических радиусов ионов в твердых телах. Радиусы ионов определяются, как правило, из условия аддитивности их в кристаллах соединений: ГАВ ГА ГВ, где ГАВ - расстояние между центрами ионов в соединении. Вообще говоря, это соотношение определяет не сами радиусы, а разность радиусов ионов В и С в соединениях АВ и АС: гдв - ГАС ГЪ-гс. Поэтому любая шкала ионных или атомных радиусов, построенная по принципу аддитивности, определяет их с точностью до некоторой достаточно произвольной постоянной ( радиус иона - эталона); аддитивность сохраняется, если радиусы всех катионов увеличить, а радиусы всех анионов уменьшить на произвольную постоянную. Более того, для описания кристаллохимии соединений с промежуточным характером связи с равным успехом можно пользоваться как ионной, так и атомной моделью строения кристалла и соответственно использовать как ионные, так и атомные радиусы, - поскольку правило аддитивности выполняется в обоих случаях. [21]
Для того чтобы оправдывалась ионная модель, силовые постоянные деформационных колебаний необходимо было уменьшить примерно на порядок. [22]
Следует отметить, что простая ионная модель, на которой основана теория кристаллического поля, не дает четкого представления о связи в соединениях переходных металлов. Имеется много экспериментальных доказательств, подтверждающих, что важную роль играют обе связи: ионная и ковалентная. Тем не менее ионная теория кристаллического поля дает простую модель, которая объясняет многие свойства переходных металлов и которая приводила и будет приводить к постановке многих экспериментов. Роль теории кристаллического поля для объяснения структуры, устойчивости и реакционной способности комплексов обсуждается в следующих главах. [23]
 |
Температурные зависимости величин и2 полных среднеквадратичных отклонений атомов различных подрешеток ( вычислены по разным отражениям одной группы для монокристаллов ферритов. [24] |
Таким образом, даже грубая, приближенная ионная модель, используемая [424] для оценки количества и разновидности дефектов, позволяет делать некоторые полуколичественные выводы о преобладающем типе точечных дефектов в шпинель-ных реальных кристаллах. [25]
 |
Зависимость геометрического строения комплексов от координационного числа центрального атома. [26] |
ТКП, исходящая из ионной модели, требует видоизменения при рассмотрении комплексов, в которых имеется заметная доля ковалентной связи. Когда эта доля сравнительно невелика, используется усовершенствованная модификация ТКП - теория поля лигандов, согласно которой наличие ковалентной связи учитывается введением определенных поправок в расчеты, проводимые методами ТКП, прежде всего на основе использования идеи перекрывания орбиталей. [27]
Сравнение с данными расчета классической ионной модели NiF64 - показывает, что хотя степень ковалентности в этом комплексе мала, она играет очень большую роль в определении разностей энергий различных состояний. Вместе с тем, оценка параметра Рака В мало отличается от полученной для чисто ионной модели. Передать энергию состояния 3Tig не удалось, по-видимому, вследствие того, что это состояние конфигурации t2g5eg3 сильно взаимодействует с таким же, по симметрии, состоянием конфигурации tzg4eg4, что должно приводить к понижению состояния 3Tig и уменьшению величины В. [28]
Наиболее убедительным аргументом против чисто ионной модели является обнаруженная в спектрах парамагнитного резонанса сверхтонкая структура от соседних ядер, недвусмысленно демонстрирующая наличие неспаренных электронов на лигандных ионах. [29]
Известны теоретические ( вычисленные по ионной модели) и экспериментальные значения ди-польного момента молекул. [30]
Страницы: 1 2 3 4