Бартел
Cтраница 3
Теперь вернемся к обсуждению ускоряющего эффекта у-дейтерирова-ния, который на первый взгляд кажется удивительно большим. Для объяснения этого явления Леффек с сотрудниками [160] предполагает, что отщепляющаяся группа в переходном состоянии затрудняет за счет пространственных факторов колебания метильной группы. Бартел [67] также объясняет наблюдаемый эффект пространственными факторами, однако при этом он исходит из совершенно другой модели переходного состояния. [31]
Бартела и заменяя уксуснокислый натрий ( который разлагается выше 300 с выделением угля) смесью уксуснокислого калия и натрия 2 превращает метан в ацетилен пропусканием метана над солями щелочноземельных металлов, или пропусканием через трубку при высоких температурах смеси метана и азота. [32]
В учебниках по химии поверхностных явлений 3 процесс смачивания поверхности твердого тела характеризуется величинами поверхностного натяжения, межфазного натяжения и краевого угла. Подобный же подход применим к твердому телу в виде порошкового продукта. Остерхоф и Бартел 5 предложили удачную классификацию процессов смачивания, в которой рассматриваются три отдельных процесса. [33]
Бартел [65-68] подробно рассмотрел возможную роль взаимодействий валентно несвязанных атомов в появлении вторичных изотопных эффектов. Метод, который он при этом использовал, до некоторой степени аналогичен изложенному в разд. Специфическим в расчете Бартела является то, что он вычислял среднее по низшему колебательному уровню значение потенциальной энергии взаимодействия не связанных между собой атомов Н - - - Н, С - - - НиС - - - Св исходном соединении, а также в продукте реакции или модели переходного состояния. Влияние изотопного эффекта на разность получающихся средних значений определяется просто величиной А81 / из уравнения ( II1 - 28), причем в качестве внутренних координат используют смещения от равновесных расстояний между несвязанными атомами. [34]
По его мнению, снижение устойчивости при переходе к недейтерированному соединению в случае такого пространственно напряженного комплекса, как ( СНз) зВ: N ( CH3) 3, связано с увеличением отталкиваний несвязанных атомов в недейтерированном соединении. Следует, однако, отметить, что величина изотопного эффекта, следующая из расчетов Бартела, решающим образом определяется выбранным значением длины В - N-связи. Поскольку точная структура комплекса не известна, а также принимая во внимание недостатки, свойственные расчетам по методу Бартела ( разд. IIIB, 1), можно заключить, что относительная роль эффектов гиперконъюгации и несвязанных взаимодействий для данного равновесия остается неизвестной. [35]
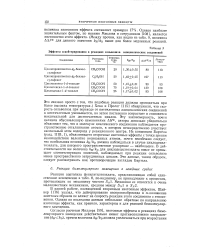 |
Эффекты а-дейтерирования в реакциях сольволиза алициклических соединений. [36] |
Это связано просто с тем, что подобные реакции должны проводиться при более высоких температурах. Хекк и Прелог [115] обнаружили, что скорость сольволиза при переходе от пятичленных алициклических соединений к шестичленным уменьшается, но затем постепенно возрастает и становится максимальной для десятичленных циклов. Эту закономерность, почти целиком обусловленную изменениями ДЯ, авторы довольно убедительно объясняют тем, что в молекуле циклического соединения наблюдается пространственное отталкивание атомов, в котором непосредственно участвует аксиальный атом водорода у реакционного центра. Из концепции Бартела ( разд. IIIB, 1), объясняющего вторичные изотопные эффекты с точки зрения взаимодействия валентно несвязанных атомов, почти неизбежно следует, что наибольшая величина & H / & D должна наблюдаться в случае циклодецил-тозилата, для которого пространственное ускорение - наибольшее. В действительности же величина & H / & D для циклодецилтозилата вовсе не превышает соответствующих значений, наблюдаемых при реакции сольволиза менее пространственно затрудненных циклов. Эти данные, таким образом, следует рассматривать как противоречащие взглядам Бартела. [37]
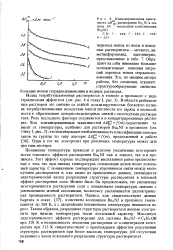 |
Концентрационная зависимость Д с растворения Bu4NJ в этаноле ( т - моляльная концентрация Bu4NJ. [38] |
Понижение температуры приводит к резкому увеличению экзотермич-ности теплового эффекта растворения Bu4NJ как в этаноле, так и в пропаноле. Этот эффект хорошо подтверждает высказанное ранее предположение о том, что при низких температурах сольватация ионов носит локальный характер. С понижением температуры упрочняются связи между молекулами растворителя и, как видно из приведенных данных, уменьшается эндотермический вклад разрушения структуры растворителя в тепловой эффект растворения соли. Можно было бы предположить, что увеличение экзотермичности растворения соли с понижением температуры связано с уменьшением ионной ассоциации, поскольку увеличивается диэлектрическая проницаемость растворителя. Однако, как свидетельствуют данные Бартела и соавт. К, а с дальнейшим понижением температуры начинается их рост. Таким образом, разрушение структуры растворителя ионами электролита при низких температурах носит локальный характер. [39]
Поэтому необходимо, чтобы пространственное сжатие в переходном состоянии увеличилось, что, по-видимому, вполне правдоподобно. Тот же результат можно было получить при использовании потенциальной функции Бартела, положительная вторая производная которой преобладает в своем влиянии над отрицательной первой производной. В данном случае трудно определить, какой из этих подходов является более правильным. Первый из них ближе к методу, использованному при рассмотрении изотопных эффектов в дипольных моментах, и основан на принятой нами простой модели. Однако он будет непригодным, если расчеты для аммиака, выполненные Бартелом [ 24а ], окажутся верными ( см. второе примечание на стр. [40]
Из работы Бартела следует, что при обсуждении природы вторичных изотопных эффектов нельзя игнорировать взаимодействия между валентно несвязанными атомами. Однако количественная сторона его расчетов отнюдь не безупречна. Вильсон [69] отметил, что в отношении сил, действующих между несвязанными атомами внутри данной молекулы, известно по существу очень мало. В настоящее время во многих, если не в большинстве, случаях нет твердой уверенности в том, имеют ли эти силы характер отталкивания или притяжения. Кроме того, если даже согласиться с тем специфическим видом функции, которую отстаивает Бартел, то все равно пренебрежение линейными и перекрестными членами выглядит неоправданным. На примере вторичного изотопного эффекта первого рода, наблюдающегося в реакции сольволиза тозилата [ см. разд. [41]
Концентрации озона у поверхности земли изменяются в разных областях в сравнительно широких пределах. Исследования, проведенные в 50 - х годах, показали [425], что в некоторых областях, в частности в районе Лос-Анжелоса, концентрации озона могут иногда значительно превышать ранее найденные значения. Сообщалось [427], что в периоды большого смога в атмосфере Лос-Анжелоса содержится 50 - 90 частей озона в 100 млн. частей воздуха. Рензетти [428] опубликовал недавно результаты работ по определению концентрации озона в атмосфере Лос-Анжелоса, причем он связывает высокие концентрации озона в воздухе с состоянием воздухоочистки. Бартел и Темпл [429] опровергли предположение о том, что перекисные соединения, образующиеся при действии озона на ненасыщенные углеводороды, присутствующие в смоге, вызывают растрескивание резины: перекисные фракции смога Лос-Анжелоса, собранные путем намораживания, как оказалось, не вызывают растрескивания. Представляют также интерес работы Гааген-Смита [430, 431], который показал, что смеси низкомолекулярных углеводородов и двуокиси азота, присутствующие в воздухе в небольших концентрациях, могут способствовать образованию озона в результате протекания фотохимических реакций. [42]
Это связано просто с тем, что подобные реакции должны проводиться при более высоких температурах. Хекк и Прелог [115] обнаружили, что скорость сольволиза при переходе от пятичленных алициклических соединений к шестичленным уменьшается, но затем постепенно возрастает и становится максимальной для десятичленных циклов. Эту закономерность, почти целиком обусловленную изменениями ДЯ, авторы довольно убедительно объясняют тем, что в молекуле циклического соединения наблюдается пространственное отталкивание атомов, в котором непосредственно участвует аксиальный атом водорода у реакционного центра. Из концепции Бартела ( разд. IIIB, 1), объясняющего вторичные изотопные эффекты с точки зрения взаимодействия валентно несвязанных атомов, почти неизбежно следует, что наибольшая величина & H / & D должна наблюдаться в случае циклодецил-тозилата, для которого пространственное ускорение - наибольшее. В действительности же величина & H / & D для циклодецилтозилата вовсе не превышает соответствующих значений, наблюдаемых при реакции сольволиза менее пространственно затрудненных циклов. Эти данные, таким образом, следует рассматривать как противоречащие взглядам Бартела. [43]
Страницы: 1 2 3