Барьер - инверсия
Cтраница 1
 |
Диаграмма, иллюстрирующая инверсию аммиака. [1] |
Барьер инверсии значительно выше для ряда соединений. [2]
Барьеры инверсии в диазиридинах весьма велики ( табл. 7) и в некоторых случаях достаточны для разделения инвертомеров при комнатной температуре. [3]
Барьер инверсии кресла должен быть достаточно низким, поскольку даже при - 104 С не наблюдалось расщепления сигналов в ПМР-спектре на сигналы аксиальных и экваториальных протонов. [4]
Барьер инверсии кресла должен быть достаточно низким, поскольку даже при - 104 С не наблюдалось расщепления сигналов протонов в спектре ПМР на сигналы аксиальных и экваториальных протонов. [5]
Барьер инверсии кресла должен быть достаточно низким, поскольку даже при - 104 С не наблюдалось расщепления сигналов в ПМР-спектре на сигналы аксиальных и экваториальных протонов. [6]
Барьеры инверсии азота составляют 5 - 6 ккал / моль [3]; соответствующие процессы являются быстрыми в шкале метода ЯМР. [7]
Барьер инверсии кольца в tyuc - гидриндане на основании низкотемпературных спектров ЯМР ( разд. Причину этого можно легко уяснить, рассматривая модели Дрейдинга: в z iic - гидриндане шестичленное кольцо выплощено и напряжено, что приводит к повышению энергетического уровня основного состояния. Однако для переходного состояния при инверсии кольца соответствующего увеличения энергии не происходит. Последнее, как уже отмечалось ( стр. Вполне очевидно, что если энергия основного состояния повышается, а энергия переходного состояния при инверсии остается прежней, энергия активации инверсии tyuc - гидриндана становится меньше соответствующей энергии циклогексана. [8]
Барьер инверсии азота в гидразине выше, чем в аммиаке и метиламине, поскольку известно, что появление гетероатома при азоте повышает барьер [12, 13] вследствие, во-первых отрицательного индуктивного эффекта заместителя и во-вторых, увеличения электростатического отталкивания неподеленных пар в переходном состоянии по сравнению с основным. Оценка экспериментальными методами относительной важности обоих эффектов затруднительна, так как они действуют в одном направлении. [9]
Относительно невысокий барьер инверсии в NH3 объясняет отсутствие оптической изомерии в аминопроизводных. Однако при переходе к этиленимину резко увеличивается этот барьер. Доказано, что этилениминопроизводные могут обладать оптической активностью. [10]
Барьер инверсии атома азота обычно связывают с энергией, необходимой для регибридизации орбитали НП из близкой к sp3 в пирамидальной конфигурации до чистой р в плоском переходном состоянии. Поскольку второй атом азота в гидразине имеет большую электроотрицательность по сравнению с водородом, а также является донором р-электронов, можно было бы ожидать, что барьер инверсии в гидразине будет заметно выше, чем в аммиаке. По-видимому, в равновесной поворотной конформации молекулы гидразина вследствие ортогональной ориентации НП изменение их взаимодействия в ходе инверсии невелико и мало сказывается на величине барьера, а различие в электроотрицательностях азота и водорода проявляется только в небольшом его увеличении. [11]
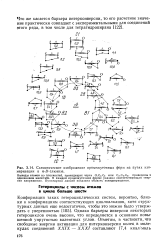 |
Схематическое изображение промежуточных форм на путях изомеризации в а - Л - глюкозе. [12] |
Однако барьеры инверсии некоторых гетероциклов очень высоки, что определяется в основном повышенной упругостью валентных углов. [13]
Уменьшение барьера инверсии в формамиде и цианамиде свидетельствует о существенном взаимном влиянии аминогруппы и присоединенных групп. Обычно оно рассматривается как проявление сопряжения. [14]
Следовательно, барьер инверсии характеризует способность атома изменять свое валентное состояние под влиянием соседних атомов и групп атомов. [15]
Страницы: 1 2 3 4