Дипольный момент - растворитель
Cтраница 2
Из этих данных следует, что максимум поглощения смещается тем больше в коротковолновую область, чем больше дипольный момент растворителя [ А. В отличие от ионов атомы галогенов, входящие в состав молекул, почти не смещают спектра. [16]
Исследование зависимости со22 ( / -) от концентрации выполнено Гольд-маном [26] для модели раствора леннард-джонсовских частиц в растворителе с потенциалом Штокмайера при Оц а220 30нм и дипольном моменте растворителя, соответствующем дипольному моменту воды. В этой работе интересны два результата. [17]
Соответствующие физические свойства растворителей собраны в приложении 1 ( в конце обзора), куда включены данные по температуре кипения, температуре замерзания, давлению паров, плотности, показателю преломления, вязкости, диэлектрической постоянной и дипольному моменту растворителей. [18]
Для ацетилацетонатов Си, Mn ( II), Co ( II), Mn ( III), Co ( III), Cr ( III) и Fe ( III) показано, что с увеличением дипольных моментов проявляющих растворителей Rf хелатов увеличивается. [19]
Нивелирующе-дифференцирующее действие растворителя зависит от ряда факторов, к числу которых ( наряду с сольватирующей способностью растворителя, склонностью к образованию водородных связей, способностью молекул и ионов растворителя и растворенного вещества к ассоциации и комплексообразованию, диэлектрической проницаемостью, полярностью, дипольным моментом растворителя и др.) в первую очередь относятся следующие. [20]
На избирательность растворителя также влияют величина ди-польного момента и характер углеводородного радикала. При постоянном углеводородном радикале избирательность увеличивается с ростом дипольного момента растворителя. Влияние функциональной группы может сглаживаться влиянием различных радикалов. Очевидно, растворитель обладает хорошей избирательностью лишь при определенном сочетании величины углеводородного радикала я вида полярной лруппы. [21]
Имеется большое число работ, в которых была ошибочно определена роль растворителя. Ранее было широко распространено представление, что адсорбируемость вещества не зависит ни от способности растворителя поглощаться адсорбентом, пи от его адсорбционного средства, ни от дипольного момента растворителя. [22]
Эти растворители обладают различными физическими и химическими свойствами, что позволило исследовать влияние на характер взаимодействия ионов с молекулами воды таких факторов, как диэлектрическая проницаемость и дипольный момент растворителя, протоно-акцепторные свойства его молекул. [23]
При наличии полярных хромофорных групп, например карбонильной группы, получается заметное смещение под влиянием растворителей с сильными молекулярными полями - имеющими бофшой дипольный; или квадрупольный момент. Согласно Шейбе ( 1925), при различных хромофорах смещение полярными растворителями происходит в различных направлениях J оно может быть и бато - и гипсохромным, а при одинаковых хромофорах2 степень смещения полосы поглощения прежде всего зависит от величины дипольного момента растворителя. Однако, наряду с этим ясно сказываются и стерические влияния экранирование неполярными группами, в первую очередь алькильными: в некоторых гомологических рядах при одинаковом дипольном моменте смещение становится постепенно меньше, вследствие усиления пространственного экранирования полярной группы растворителя, например, в гомологическом ряду спиртов 3 или такого же экранирования хромофора, например, в гомологическом ряду кетонов. [24]
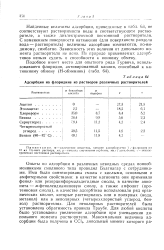 |
Адсорбция на флоридине из растворов различных растворителей. [25] |
Найденные величины адсорбции, приведенные в табл. 63, не соответствуют растворимости воды в соответствующем растворителе, а также диэлектрической постоянной растворителя. С изменением поверхности натяжения ( для поверхности раздела вода - растворитель) величины адсорбции изменяются, по-видимому, симбатно. Зависимость этих величин от дипольного момента растворителя не ясна. [26]
Для неполярных растворителей установлена обратимость правила Траубе. Адсорбция увеличивается при уменьшении дипольного момента растворителя. Наибольшая адсорбция наблюдается из четыреххлористого углерода; дипольный момент его равен нулю. [27]
Наряду с химическими на растворимость влияют также и физические факторы. Так как растворение вещества чаще всего является эндотермическим процессом, с увеличением температуры растворимость возрастает. Поскольку для растворимости гетерополярного соединения наряду с другими факторами решающими являются диэлектрическая проницаемость и дипольный момент растворителя, то растворимость его зависит также и от природы растворителя. [28]
Наряду с химическими на растворимость влияют также и физические факторы. Так как растворение вещества чаще всего является эндотермическим процессом, с увеличением температуры растворимость возрастает. Поскольку для растворимости гетерополярного соединения наряду с другими факторами решающими являются диэлектрическая проницаемость и дипольный момент растворителя, то растворимость его зависит также и от природы растворителя. [29]
Было показано, что инфракрасная полоса поглощения CH3OD, растворенного в бензоле, имеет частоту, почти равную частоте полосы, получающейся в парообразном CH3OD, но что при растворении его в основных или амфи-протических растворителях происходит сдвиг к более низким частотам, сопровождающийся расширением и повышением интенсивности полосы. Как удалось показать, это явление объясняется образованием дейтериевых связей или мостиков, а потому степень сдвига частоты была с вполне достаточным основанием признана мерой донорных свойств растворителя. Авторы считают, что это допущение находит подтверждение в том факте, что между наблюдаемыми сдвигами частоты и дипольными моментами растворителей нет никакой зависимости, тогда как из 20 исследованных оснований между этими сдвигами и логарифмами констант основности была обнаружена линейная зависимость в 17 случаях. [30]
Страницы: 1 2 3