Дипольный момент - растворитель
Cтраница 3
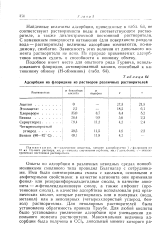 |
Адсорбция на флоридине из растворов различных растворителей. [31] |
Ими были синтезированы смолы с кислыми, основными и амфотерными свойствами: в качестве катионита они применяли фенол - или резорцинформальдегидные смолы, в качестве анио-нита - ж-фенилендиаминовую смолу, а также амфолит ( протеиновая смола), в качестве адсорбтива использовали ряд органических кислот, которые растворялись или в полярных ( вода, метанол) или в неполярных ( четыреххлористый углерод, бензол) растворителях. Для неполярных растворителей была установлена обратимость правила Траубе. Для любой кислоты было установлено увеличение адсорбции при уменьшении дипольного момента растворителя. [32]
При этом смещается также положение максимума ( 320, 330, 340 нм) в сторону длинных волн, что указывает на изменение степени конденсированно-сти ароматических соединений. Полоса 410 нм отнесена к п - - п - лереходам, которые возможны в гетероатомных соединениях. При зтом следует иметь в виду, что интерпретируемые УФ-спектры были получены на образцах асфальтенов, подвергавшихся термическому воздействию ( при 120, 240 и 560 С) при их фракциони-ровке, и, вероятно, претерпевших существенные структурно-химические изменения. Следует отметить, что такие тщательные методические разработки в этих исследованиях, как учет диэлектрической проницаемости и дипольного момента растворителей при получении спектров, а также получение квазилинейчатых спектров поглощения асфальтенов ( 415, 418, 425, 434 нм) при замораживании их нитробензольных растворов в матрице м-гексана ( - 196 С) ( рис. 40), заслуживают внимания и ждут объяснения. [33]
На первой стадии диспергирования раствор полимера должен смочить поверхность пигмента. При смачивании пигментов и наполнителей происходит вытеснение с их поверхности одних веществ другими. Например, вода и газы, адсорбированные поверхностью пигмента, могут быть вытеснены органическими растворителями. Смачивание сопровождается тепловым эффектом. Чем лучше растворитель смачивает поверхность, тем выше теплота смачивания; к тому же чем выше дипольный момент растворителя, тем выше теплота смачивания. Наличие прямой пропорциональности между этими величинами объясняется действием электростатических сил на поверхности пигментов. [34]
 |
Дипольные моменты и поляризуемость некоторых молекул. [35] |
Значения дипольных моментов дают информацию о строении молекул и, кроме того, часто используются для проверки того, насколько верно вычислены молекулярные орбнтали. На практике знание величин дипольных моментов необходимо, например, для подбора подходящего растворителя для данного твердого вещества, так как способность растворителя разрушать ионные кристаллы связана с его способностью сольватировать ионы и уменьшать электростатическое взаимодействие, удерживающее ионы в кристалле. Роль полярных молекул растворителя двойная. Во-первых, один конец диполя молекулы растворителя может электростатически притягиваться к иону противоположного знака, и это уменьшает энергию иона. Во-вторых, в растворе уменьшается сила кулоновского взаимодействия между ионами. Это достигается следующим образом. Когда два иона находятся в вакууме на расстоянии R друг от друга, потенциальная энергия их взаимодействия пропорциональна s R, где SQ - диэлектрическая проницаемость вакуума ( 8.854 10 Дж Кл м); однако, когда оии помещены в растворитель, энергия уменьшается до l / 4TiS ( sR, где s - относительная ( если принять SQ за единицу) диэлектрическая проницаемость растворителя. Величина s частично определяется дипольным моментом растворителя, и может оказать большое влияние на силу кулоновского взаимодействия. Например, вода имеет s78; это значит, что кулоновское взаимодействие в воде уменьшается почти на два порядка по сравнению с вакуумом. [36]
Страницы: 1 2 3