Дипольный момент - связь
Cтраница 2
Дипольные моменты связей углерода с другими атомами тем больше, чем правее стоит элемент в ряду периодической системы. Связь атома углерода с атомом фтора более полярна, чем связь с атомом кислорода, а последняя более полярна, чем связь с атомом азота. [16]
 |
Векторное изображение дипольных моментов. [17] |
Дипольные моменты связей углерода с другими атомами тем больше, чем правее стоит элемент в периодической системе. Связь атома углерода с атомом фтора более полярна, чем связь с атомом кислорода, а последняя более полярна, чем связь с атомом азота. [18]
Дипольный момент связи карбонильной группы доходит до 2 7 D, а в спиртах всего около 1.7 D. Такая высокая поляризация определяет электрофильные свойства углерода карбонильной группы и его способность реагировать с нуклеофильными соединениями, например присоединять анионы реагирующей молекулы. Кислород карбонильной группы обладает нуклеофильными свойствами. Примеры подобных реакций приведены ниже. [19]
Вычислите дипольный момент связи хлор - углерод, представив дипольный момент для о - и ж-изомеров как сумму двух векторов, расположенных друг относительно друга под углом 60 и 120 соответственно. [20]
Поскольку дипольный момент связи С - Н неизвестен, вычисления производились при трех предположениях о величине этого момента в метане: а 0 3 дебая, ц, 0 и ц - 0 3 дебая. [21]
Хотя дипольный момент связи С-F значителен, сумма моментов равна нулю, так как они скомпенсированы. [22]
Чем больше дипольный момент связи С - Н, тем больше дробный положительный заряд на атоме водорода, - тем больше протонизирован атом водорода. [23]
Компенсация дипольных моментов связей широко распространена среди углеводородов. Метиль-ная группа в целом обладает таким же моментом, поэтому во всех предельных углеводородах эти моменты полностью взаимно компенсируются при любом строении молекул этих углеводородов. [25]
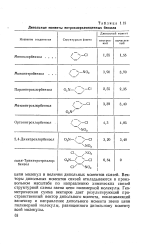 |
Дипольные моменты нитрохлорзамещенных бензола. [26] |
Векторы дипольных моментов связей откладываются в произвольном масштабе по направлению химических связей структурной схемы звена цепи полимерной молекулы. Геометрическая сумма векторов дает результирующий пространственный вектор дипольного момента, показывающий величину и направление дипольного момента звена цепи полимерной молекулы, равноценного дипольному моменту всей молекулы. [27]
Значения дипольных моментов связей, используемые при расчетах, не следует рассматривать как всегда постоянные величины. При переходе к более сложным соединениям они могут принимать иные значения. [28]
Таблица дипольных моментов связи составлена в предположении, что суммарный дипольный момент молекулы есть векторная сумма диполей, соответствующих отдельным связям. На основе приведенных ниже данных и табл. 5.1 проверьте, существует ли корреляция между дипольным моментом связей и электроотрицательностью. [29]
Зависимость дипольного момента связи в этом случае имеет селективный характер [13], и малое смещение Sbn из центрального положения равновесия приводит к большому дипольному моменту элементарной ячейки. [30]
Страницы: 1 2 3 4
