Моногалогениды
Cтраница 2
Наиболее типичны моногалогениды для таллия. Монофторид легко получить, нейтрализуя гидроксид таллия Т1ОН плавиковой кислотой. Он хорошо растворим в воде и может быть обезвожен переплавкой. Растворимость остальных моногалогенидов ( получаются прямым синтезом) мала и падает от хлорида к иодиду. В этом отношении моногалогениды таллия напоминают галогениды серебра. Сходство еще более усиливается светочувствительностью галогени-дов таллия и окраской их кристаллов: Т1С1 - бесцветный, TIBr - бледно-желтый, T1I имеет две модификации - желтую и красную. Карбонат таллия ( 1) хорошо растворяется в воде, подобно карбонатам щелочных металлов, и дает щелочную реакцию. Таким образом, в степени окисления 1 таллий ведет себя и как серебро, и как щелочной металл. [16]
Наиболее типичны моногалогениды для таллия. Монофторид легко получить, нейтрализуя гидроксид таллия Т1ОН плавиковой кислотой. Он хорошо растворим в воде и может быть обезвожен переплавкой. Растворимость остальных моно-галогенидов ( получаются прямым синтезом) мала и уменьшается от хлорида к иодиду. В этом отношении моногалогениды таллия напоминают галогениды серебра. Сходство еще более усиливается фоточувствительностью галогенидов таллия и окраской их кристаллов: Т1С1 - бесцветный, Т1Вг - бледно-желтый, T1I имеет две модификации - желтую и красную. Карбонат таллия ( 1) хорошо растворяется в воде, подобно карбонатам щелочных металлов, и дает щелочную реакцию. Таким образом, в степени окисления 1 таллий ведет себя и как серебро, и как щелочной металл. [17]
Обычно получается моногалогенид, однако в некоторых случаях этим путем можно получить дигалогенид; следует принимать меры, чтобы избежать излишнего отщепления. [18]
Таким образом, непредельные моногалогениды винильного типа I ( способы получения которых рассмотрены на стр. Многостадийность и сложность всего процесса являются, по-видимому, препятствием для применения этого ряда реакции в качестве препаративного метода получения алкинов. Действием цинка на непредельные 1 2-дибромиды были получены с невысокими выходами пентин-1, 4-метилпентин - 1ш - Г 9, гексин - 31Н1 ьо. [19]
ПА и IIIA, остальные моногалогениды этих металлов, а также серебра и таллия, галогениды МХ2 или МХ3 других металлов, обведенных сплошными линиями в табл. 7.1. Очевидно, что вне этого перечня остаются большие группы соединений ( среди них даже бинарные), которые также должны быть учтены в любом достаточно детальном обзоре химических связен в неорганических соединениях. Следует признать, что удовлетворительное и общепринятое описание связей для многих из этих групп не разработано. В соединениях этих металлов с более электроотрицательными неметаллами связи имеют, вероятно, промежуточный характер между ионными н кова-лентными, но при переходе к элементам подгрупп Б более выраженные металлические свойства полуметаллов свидетельствуют о наличии в их соединениях связей, по характеру промежуточных между ковалентной и металлической. Возникают значительные проблемы при описании связей даже в структурах самих свободных элементов этих подгрупп. [20]
Все эти элементы образуют моногалогениды ЭГ. Для алюминия эти соединения, существующие только при высоких температурах, получаются по реакциям тригалогенидов с металлом. [21]
Для серебра хорошо известны все моногалогениды, плавящиеся без разложения. В то ж е время для золота моногалогениды почти не характерны. Так, монофторид золота неизвестен, а остальные неустойчивы, даже монохлорид. Энтальпия образования Aul равна 4.0 кДж / моль. Галогениды меди занимают промежуточное положение, монофторид также не существует. Из галогенидов меди в степени окисления 2 наиболее устойчив CuF2, а иодид не получен. [22]
В кристаллическом состоянии известны все моногалогениды индия, за исключением InF, существующего только в парообразном состоянии, хотя эти соединения гораздо менее устойчивы, чем соединения таллия. Ион 1п присутствует в кристаллических InBr и Inl ( гл. [23]
Распространенное ранее представление о том, что моногалогениды меди имеют удвоенные молекулы, было основано на определении плотности их в парах, которая характеризует лишь среднюю величину частиц. [24]
Ацетилен и его гомологи, присоединяя галоидо-водород, образуют либо непредельные моногалогениды, либо предельные дигалогениды. [25]
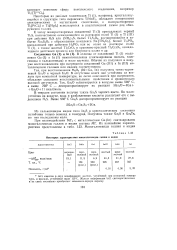 |
Некоторые характеристики моногалогенидов галлия и индия. [26] |
При взаимодействии МГ3 с металлическим Ga ( In) синтезированы моногалогениды галлия и индия состава МГ. [27]
Эр лих ( Ehrlich, 1953 - 1955), пытаясь синтезировать моногалогениды щелочноземельных металлов, не получил доказательств их существования в твердом состоянии. Эти соединения представляют собой бесцветные тетрагональные листочки, внешне напоминающие слюду. Водой они разлагаются со значительным выделением тепла. Строение их молекул аналогично BiOCl, BiOBr, BiOl ( см. стр. [28]
Дигалогенциклопропаны при действии ( С4Н) 3ЗпН или М § в СН3ОН восстанавливаются в моногалогениды, а при взаимод. [29]
Теплоты реакции такого диспропорционирования приведены в табл. 3.6, из которой следует, что моногалогениды щелочноземельных металлов неустойчивы. [30]
Страницы: 1 2 3 4