Монокальций-фосфат
Cтраница 2
В варианте, где был взят плавленый магниевый фосфат, вносившийся по MgO, недостающее количество фосфора добавлялось в виде монокальций-фосфата. Таким образом, во всех случаях внесены одинаковые количества фосфора. [16]
Влияние начальной величины Т: Ж на скорость разложения апатита фосфорной кислотой представляется весьма важным с точки зрения оценки факторов кристаллизации монокальций-фосфата. [17]
 |
Изотермы растворимости в системе MgO - РгО6 - Н2О при 25, 80 и 130 С. [18] |
Как и для солей кальция, с увеличением концентрации Р2О5 растворимость димагнийфосфата растет, а мономагнийфос-фата уменьшается ( см. рис. 4.14), но в отличие от монокальций-фосфата степень разложения водой мономагнийфосфата почти не зависит от температуры. [19]
Из диаграммы видно, что с увеличением содержания в растворе P2OS упругость пара раствора уменьшается, причем падение кривой упругости более полого в области равновесия растворов с дикальцийфосфатом, чем в области равновесия с монокальций-фосфатом. [20]
Из диаграммы видно, что с увеличением содержания в растворе Р2О3 упругость пара раствора уменьшается, причем падение кривой упругости более полого в области равновесия растворов с дикальцийфосфатом, чем в области равновесия с монокальций-фосфатом. [21]
Когда вытяжка получена разложением фосфата 50 % - ной азотной кислотой, взятой с избытком в 20 % по отношению к стехиометриче-скому количеству, то раствор, образующийся при преципитировании этой вытяжки, несколько не насыщен по отношению к монокальций-фосфату, если избыточная кислота не нейтрализована аммиаком. Таким образом, применение избытка азотной кислоты для получения вытяжки не предотвращает выделения монокальцийфосфата вследствие нейтрализации ее полностью при образовании преципитата. [22]
 |
Растворимость кремнефторида и фосфатов кальция в смесях фосфорной и азотной кислот. Изотерма 60 С. [23] |
Сопоставление степени разложения монокальцийфосфата при одинаковых весовых соотношениях соли и воды в системах СаО - Р20В - Н20 и СаО - Р205 - CaSiF6 - H20, представленное на рис. 10, показало влияние фтора на сильное увеличение степени разложения монокальций-фосфата. [24]
Монокальцийфосфат получают из апатитового концентрата или фосфоритов Каратау, а также обесфторенных термической или экстракционной фосфорных кислот и сепарированного или сухого молотого мела. Монокальций-фосфат используется в качестве фосфорно-кальциевой подкормки для всех видов животных. [25]
Во второй стадии фосфат разлагается фосфорной кислотой, и по мере увеличения степени ее нейтрализации активность раствора и скорость процесса уменьшаются. Когда жидкая фаза становится насыщенной монокальций-фосфатом, что совпадает с окончанием созревания суперфосфатной массы в камере, скорость разложения еще больше замедляется. Это обусловлено, помимо уменьшения активности жидкой фазы, тем, что во второй фазе процесса разлагаются наиболее крупные зерна фосфата, на поверхности которых могут быть шламовые покровы из кристаллов сульфата кальция. [26]
Как видно, количество оборачиваемой фосфорной кислоты в способе с циркуляцией кислоты в 3 33 раза больше, чем в обычном способе. В процессе регенерации НзРО4 также увеличивается количество обрабатываемого фосфата ( монокальций-фосфата) приблизительно в 2 5 раза по сравнению с обычным экстракционным процессом. [27]
Разложение фторапатита фосфорной кислотой протекает в две стадии. Вначале происходит нейтрализация первого иона водорода фосфорной кислоты до полного насыщения раствора монокальций-фосфатом. На рис. VI-2 момент насыщения соответствует точкам пересечения луча растворения с изотермой растворимости LBT. В дальнейшем разложение фторапатита происходит в насыщенных растворах фосфорной кислоты при выпадении в твердую фазу кристаллов монокальцийфосфата, или дикальцийфосфата, или их смеси. [28]
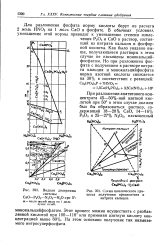 |
Водная диаграмма.| Схема циклического про. [29] |
Как было указано выше, получающиеся растворы в этом случае не насыщены монокальций-фосфатом. [30]
Страницы: 1 2 3 4